
tría por reflectancia para medir la saturación de oxígeno tisular por
debajo del sensor. Habitualmente, se aplican dos sensores colocados
a ambos lados de la frente. La luz atraviesa no sólo partes de la
porción frontal del cerebro, sino también el cráneo y el cuero cabe-
lludo que hay por encima. La contaminación de la señal de oximetría
por fuentes sanguíneas extracraneales es una seria preocupación,
aunque puede reducirse al mínimo este problema utilizando dos
diodos sensores a diferentes distancias de la fuente luminosa dentro
del área de un sensor y con ajustes del algoritmo del oxímetr
o 13,14 .Dado que entre dos tercios y cuatro quintos del volumen
sanguíneo cerebral es sangre venosa, la oximetría cerebral deter-
mina sobre todo la «saturación local de oxígeno venoso
» 15 .Se
puede esperar que ante una isquemia cerebral, los valores de oxi-
metría disminuyan como resultado de una extracción de oxígeno
aumentada, mucho antes de que falle la función o se produzca un
daño neuronal permanente. La simplicidad de su uso y la familia-
ridad con los principios de tratar disminuciones en la saturación
de oxígeno venoso sistémico han hecho de la oximetría cerebral un
popular método de monitorización en intervenciones que pueden
causar potenciales descensos del flujo sanguíneo de los vasos cefá-
licos. No obstante, existen algunas importantes limitaciones para el
uso de la oximetría cerebral durante este tipo de procedimientos.
En primer lugar, la suficiencia de la perfusión cerebral global se
extrapola a partir de medidas del parénquima cerebral fronto-
temporal. En segundo lugar, existe una ausencia notable de datos
estandarizados sobre valores normales o sobre los cambios espera-
dos en la oximetría cerebral, pero la aplicación preoperatoria de los
sensores permite iniciar la monitorización continua junto con una
exploración neurológica basal.
Como ejemplo de cómo acaban estas limitaciones se puede
citar un estudio sobre el uso de la oximetría cerebral durante 100 en
darterectomías carotídeas en pacientes despierto
s 16 .La oximetría ce-
rebral fue capaz de identificar un 97,4% de pacientes con un FSC
adecuado, tal y como indicaba la ausencia de sintomatología clínica.
Con frecuencia el monitor indicaba un FSC inadecuado, definido
como un descenso del 20% en la saturación de oxígeno cerebral a
partir del nivel basal prepinzamiento, aunque el paciente no tenía
síntomas clínicos de un FSC inadecuado. La tasa de falsos positivos
del 66,7% puede simplemente ilustrar el hecho de que la extracción de
oxígeno aumenta antes de que falle la función. El problema real es que
se desconoce el límite inferior de una saturación de oxígeno regional
aceptable en una gran población de paciente
s 17 .El valor puede variar
de un paciente a otro, y al añadir fármacos anestésicos que influyen en
el metabolismo cerebral se puede confundir aún más el cuadro.
Técnicas de monitorización (invasivas) del flujo
sanguíneo a nivel tisular
La monitorización a nivel tisular para el cerebro es, por definición,
invasiva. Todos los métodos de monitorización que actualmente se
utilizan en la clínica o en investigación se implantan a través de un
trépano, se extienden al interior de la sustancia blanca o bien al
sistema ventricular, y normalmente se utiliza un perno para la esta-
bilización. Todas estas técnicas comparten entre un 1 y un 2% de
riesgo de sangrado, infección o isquemia debido al procedimiento
de implantació
n 18 .Una segunda característica que también compar-
ten es su resolución espacial limitada (es decir, cada sonda de moni-
torización sólo monitoriza un área cerebral limitada que rodea a la
sonda). Cuando estas técnicas de monitorización se desarrollaron
por primera vez, se produjo un debate considerable acerca de la
colocación óptima del dispositivo ante tan limitada resolución espa-
cial. A partir de la apreciación actual sobre el impacto de daños
neurológicos secundarios sobre el resultado final, existe un consenso
creciente de que la monitorización a nivel tisular se realiza mejor en
tejido morfológica y funcionalmente normal que forme parte de la
zona de penumbra o de interés vulnerabl
e 19-21 .Colocar un monitor
de flujo sanguíneo en el interior del tejido cerebral irrigado por una
arteria en la que exista un aneurisma en el contexto de una hemo-
rragia subaracnoidea aumenta al máximo, aunque no garantiza las
posibilidades de detectar precozmente un vasoespasmo.
De las técnicas de monitorización de nivel tisular, dos han
experimentado un refinamiento suficiente como para que se
puedan utilizar de forma generalizada. Representan las dos princi-
pales formas de valoración de un flujo sanguíneo adecuado: la
valoración del FSC a través de la monitorización de la difusión
térmica o la valoración del suministro de oxígeno mediante la
monitorización de la presión parcial de oxígeno tisular (Po
2
).
Monitorización por difusión térmica del flujo sanguíneo
cerebral.
La monitorización del FSC por difusión térmica se basa
en la idea de que la tasa a la que se disipa el calor en un tejido
depende de las propiedades de conductividad térmica del tejido y
del flujo sanguíneo en esa zona. Dado que las propiedades de disi-
pación térmica se mantienen constantes, los cambios en la disipación
térmica reflejan cambios en el flujo sanguíneo y pueden expresarse
cuantitativamente en las unidades convencionales de FSC como
ml/100g/min. En la práctica, la sonda consiste en un catéter fino con
dos termistores colocados con una separación de 5mm
( fig. 36-2).
Cuando son insertados, ambos termistores se localizan en la sustan-
cia blanca subcortical. El termistor proximal, o pasivo, mide la tem-
peratura cerebral, mientras que el termistor distal, o activo, es
calentado 2°C por encima de la temperatura medida por el termistor
pasivo. La potencia necesaria para mantener la diferencia de tempe-
ratura de 2°C es directamente proporcional al FSC. Se utiliza la tasa
inicial de propagación del campo térmico para establecer el compo-
nente conductivo fijo de la transferencia térmica.
1246
Control de la anestesia
III
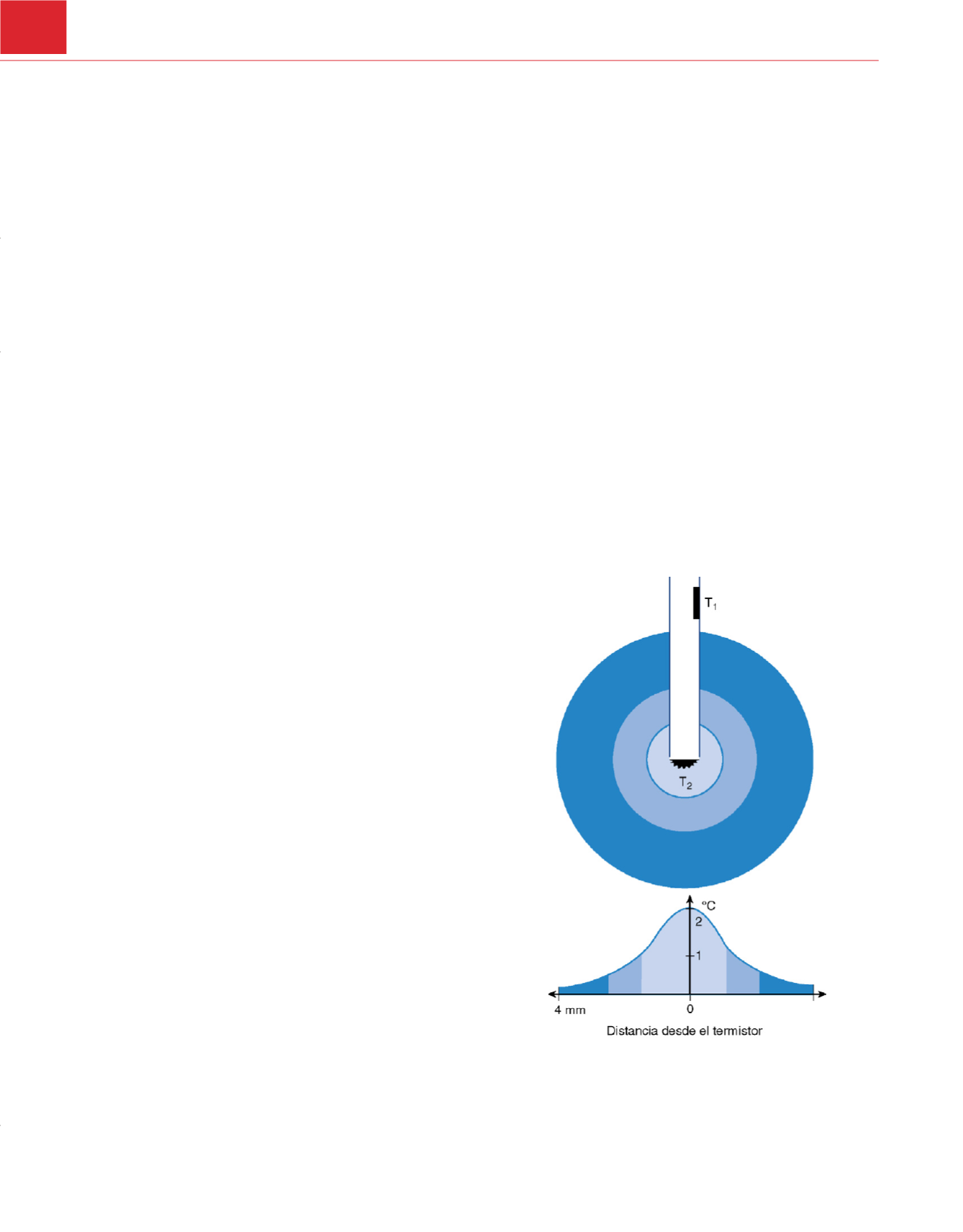
Figura 36-2
Medición de la difusión térmica del flujo sanguíneo cerebral. La
sonda se coloca en la sustancia blanca subcortical. Contiene un termistor
pasivo (T
1
) que mide la temperatura cerebral y se localiza fuera del área de
influencia del termistor activo. El termistor activo (T
2
) es calentado 2°C por
encima de la temperatura cerebral. La energía requerida para mantener ese
aumento de la temperatura es proporcional al flujo sanguíneo cerebral.









