
El espesor del músculo del VI es un modificador importante
de la tensión parietal. Por ejemplo, en la estenosis aórtica está
aumentada la poscarga. El ventrículo tiene que generar una presión
mucho mayor para superar el aumento de la carga que se opone a
la eyección sistólica de la sangre. Para generar este rendimiento tan
elevado, se produce un aumento del espesor parietal del ventrículo
(hipertrofia del VI). Aplicando la ley de Laplace, el aumento del
espesor parietal del VI reducirá la tensión parietal a pesar
del aumento necesario de la presión en el VI para superar la este-
nosis aórtica
( fig. 6-4 ) 7. En un corazón insuficiente aumenta el
radio del VI, lo que aumenta la tensión parietal.
Relación de Frank-Starling
La relación de Frank-Starling es una propiedad intrínseca del mio-
cardio mediante la cual la distensión de los sarcómeros miocárdicos
da lugar a un aumento del rendimiento miocárdico para las con-
tracciones posteriores (v.
fig. 6-3 ). Otto Frank observó por primera
vez en el músculo esquelético que la modificación de la tensión se
relacionaba directamente con su longitud, y que en el corazón, a
medida que cambiaba la presión, se producía el correspondiente
cambio de volume
n 8. E. H. Starling, utilizando una preparación de
corazón-pulmón aislados como modelo, observó en 1914 que «la
energía mecánica que se libera en el paso desde el estado de reposo
al estado contraído depende de la longitud de la fibra muscular
» 9.
Si se monta una tira de músculo cardíaco en una cámara muscular
en condiciones isométricas, el aumento de la longitud del sarcó-
mero da lugar a un aumento de la fuerza de la contracción. Starling
concluyó que el aumento de la fuerza de la contracción se debía a
la mayor interacción de los haces musculares.
La microscopia electrónica ha demostrado que la longitud
del sarcómero (2,0-2,2
m
m) se relaciona positivamente con la mag-
nitud de la formación de enlaces cruzados entre la actina y la
miosina, y que hay una longitud óptima del sarcómero a la cual la
interacción es máxima. Este concepto se basa en la suposición de
que el aumento de la formación de enlaces cruzados es equivalente
a un aumento del rendimiento muscular. Aunque esta teoría sigue
siendo cierta para el músculo esquelético, la relación fuerza-longi-
tud en el músculo cardíaco es más compleja. Cuando se comparan
las relaciones fuerza-longitud del músculo esquelético y el músculo
cardíaco, se debe señalar que la reducción de la fuerza es de tan
sólo el 10% aunque el músculo cardíaco esté al 80% de la longitud
del sarcómer
o 8. Se sigue investigando la base celular del mecanismo
de Frank-Starling, que se analizará brevemente más adelante. Una
aplicación clínica frecuente de la ley de Starling es la relación
del volumen telediastólico ventricular izquierdo (VTDVI) con el
volumen sistólico. El mecanismo de Frank-Starling puede perma-
necer intacto incluso en un corazón insuficient
e 10 .Sin embargo, el
remodelado ventricular después de una lesión o en la insuficiencia
cardíaca puede modificar la relación de Frank-Starling.
Contractilidad
Cada una de las curvas de Frank-Starling especifica un nivel de
contractilidad, o el estado inotrópico del corazón, que se define
como el trabajo que realiza el músculo cardíaco a cualquier
volumen telediastólico dado. Los factores que modifican la con-
tractilidad crearán una familia de curvas de Frank-Starling con
diferente contractilidad
( fig. 6-5 ) 7. Se sabe que el ejercicio, la esti-
162
Fisiología y anestesia
I
Figura 6-3
Relación de Frank-Starling. Se muestra
la relación que hay entre la longitud del sarcómero
y la tensión desarrollada en el músculo cardíaco.
En el corazón, un aumento del volumen
telediastólico es el equivalente al aumento de la
fuerza miocárdica; por tanto, según la ley de
Starling, se genera un aumento del volumen
sistólico.
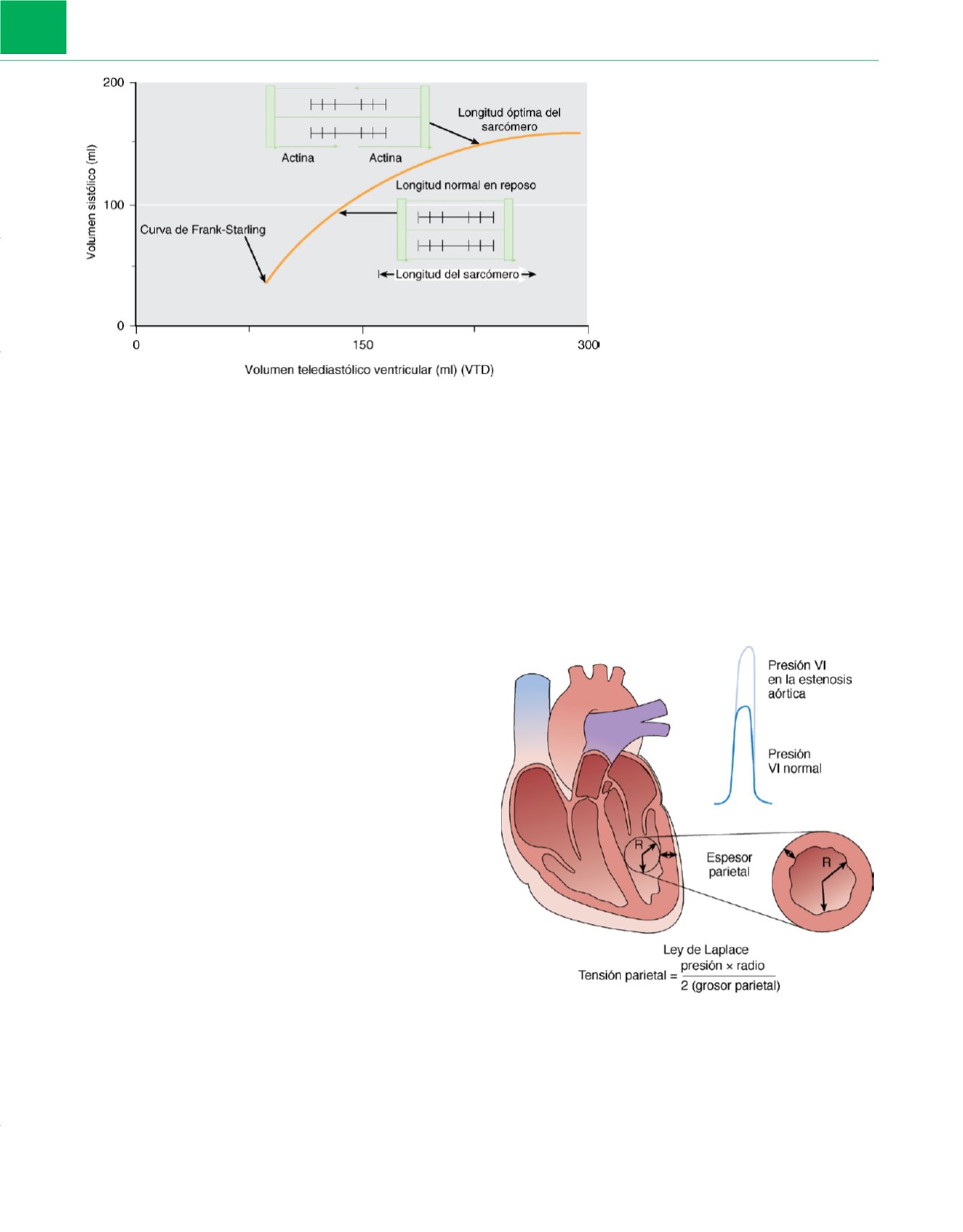
Figura 6-4
En respuesta a la estenosis aórtica aumenta la presión ventricular
izquierda (VI). Para mantener la tensión parietal en niveles controlados se
produce hipertrofia compensadora del VI. Según la ley de Laplace, tensión
parietal=presión×radio ÷ (2×espesor parietal). Por tanto, el aumento del
espesor parietal compensa el aumento de la presión, y se mantiene la tensión
parietal en niveles controlados.
(De Opie LH: Ventricular function.
En The
Heart. Physiology from Cell to Circulation,
4.
a
ed. Filadelfia, Lippincott-Raven,
2004, págs. 355-401.)









