
sina, que modula el tono arteriolar eferente y aferente, así como el
FG (v. más adelante).
Mecanismos de control arteriolar aferente y eferente
Un determinante básico del FG es la presión de filtración glomeru-
lar, que depende no sólo de la presión de perfusión de la arteria
renal, sino también del equilibrio entre el tono arteriolar aferente
y eferente. En el caso de una disminución de la presión o del flujo
sanguíneo en la arteriola aferente, los bajos niveles de catecolami-
nas, angiotensina y arginina vasopresina (AVP) inducen sobre todo
una constricción arteriolar eferente, que mantiene la presión de
filtración glomerular
( fig. 8-4A). Esta respuesta adaptativa se refleja
en un aumento de la fracción de filtración (FF) calculada, que es
el FG expresado como una fracción del flujo plasmático renal
(FPR): FF=FG/FPR. La elevación de los niveles de catecolaminas
y angiotensina (pero no de AVP) aumenta el tono arteriolar afe-
rente y disminuye la presión de filtración glomerular (y el FG) de
forma desproporcionada con el FPR, por lo que la FF disminuye
( fig. 8-4 B).
Retroalimentación tubuloglomerular
La retroalimentación tubuloglomerular puede ser un mecanismo
primordial de la autorregulación rena
l 3. Cuando el FG aumenta,
llega más NaCl al túbulo distal. La mácula densa detecta el aumento
del cloruro (Cl
−
) y desencadena la liberación de renina a partir de
la arteriola aferente adyacente. Se elabora angiotensina y se produce
constricción arteriolar, que disminuye el FG.
Durante la isquemia del asa gruesa ascendente cesa la reab-
sorción de NaCl, se pierde la capacidad del túbulo para concentrar
la orina y, en teoría, se produce una poliuria refractaria. Thurau y
Boylan
5sugirieron que un mayor aporte de NaCl a la mácula densa
desencadena una constricción arteriolar mediada por angioten-
sina, que disminuye el FG, causa oliguria, conserva el volumen
intravascular y protege al organismo de la deshidratación (la
llamada suficiencia renal aguda).
Autorregulación renal
La autorregulación permite al riñón mantener un ajuste de los
solutos y el agua con independencia de las amplias fluctuaciones
de la presión arterial. En 1951, los estudios clásicos en perros de
Shipley y Stud
y 6demostraron que este órgano mantiene un flujo
sanguíneo renal (FSR) y un FG constantes a lo largo de un rango
de presión arterial de 80-180 mmHg
( fig. 8-5). La diuresis no está
sujeta a autorregulación. La reabsorción tubular de agua determina
la diuresis, que está estrechamente relacionada con la presión
hidrostática en los capilares peritubulares. La hipotensión, ya sea
inducida o involuntaria, produce una disminución de la diuresis
que sólo puede corregirse cuando se normaliza la presión arterial.
Hay evidencias considerables que apoyan la existencia de
dos mecanismos principales en la autorregulación rena
l 3 .A me
dida que la presión arterial media disminuye, la resistencia vascu-
lar renal se reduce y el FSR se mantiene. La explicación más
plausible es una respuesta miogénica en la cual las arteriolas
sufren vasoconstricción en respuesta al aumento de la presión
arterial y viceversa. También puede participar la retroalimenta-
ción tubuloglomerular a través del aparato yuxtaglomerula
r 3,4,7.
Cuando la presión arterial aumenta en el rango de autorregula-
ción, se eleva el aporte de cloruro sódico a los quimioreceptores
de la mácula densa, la cual genera trifosfato de adenosina (ATP)
y adenosina que estimulan el receptor de adenosina A
1
e inducen
vasoconstricción de la arteriola aferente
( fig. 8-6). Esto, a su vez,
disminuye el FSR y el FG hasta los niveles previos. Ocurre el efecto
opuesto cuando disminuye la presión arterial. La liberación local
de óxido nítrico atenúa la retroalimentacion tubuloglomerular,
mientras que la liberación de angiotensina II la potenci
a 4 .El bloqueo de los canales de calcio altera la autorregulación,
lo que implica que existe un mecanismo dependiente de calcio que
está involucrado, pero esto no ocurre con la mayoría de los agentes
anestésicos. Hay un reajuste de la autorregulación en la hiperten-
sión arterial crónica que puede perderse en el riñón diabético.
Existe evidencia experimental de que se pierde la autorregulación en
el fracaso renal agud
o 8 ;esto puede deberse en parte a disfunción
endotelial debido a un exceso de óxido nítrico porque hay una
activación de la sintetasa de óxido nítrico provocada por la lesión
de isquemia-reperfusión
. 9Se observa la dependencia de la presión
sanguínea del FSR durante la circulación extracorpórea (CEC
) 10y
en la sepsis grav
e 11, pero esto puede ser debido sencillamente a
hipotensión por debajo del rango de autorregulación, más que
Fisiología renal
211
8
Sección I
Fisiología y anestesia
© ELSEVIER. Fotocopiar sin autorización es un delito
Figura 8-5
Autorregulación del filtrado glomerular (FG) y del flujo sanguíneo
renal (FSR). El FG y el FSR permanecen constantes entre unas presiones
arteriales renales de 80-180 mmHg.
(Basada en el estudio original de Shipley
and Study
5
. De Pitts RF:
Physiology of the Kidney and Body Fluids
. Chicago,
Year Book, Medical Publishers, 1974.)
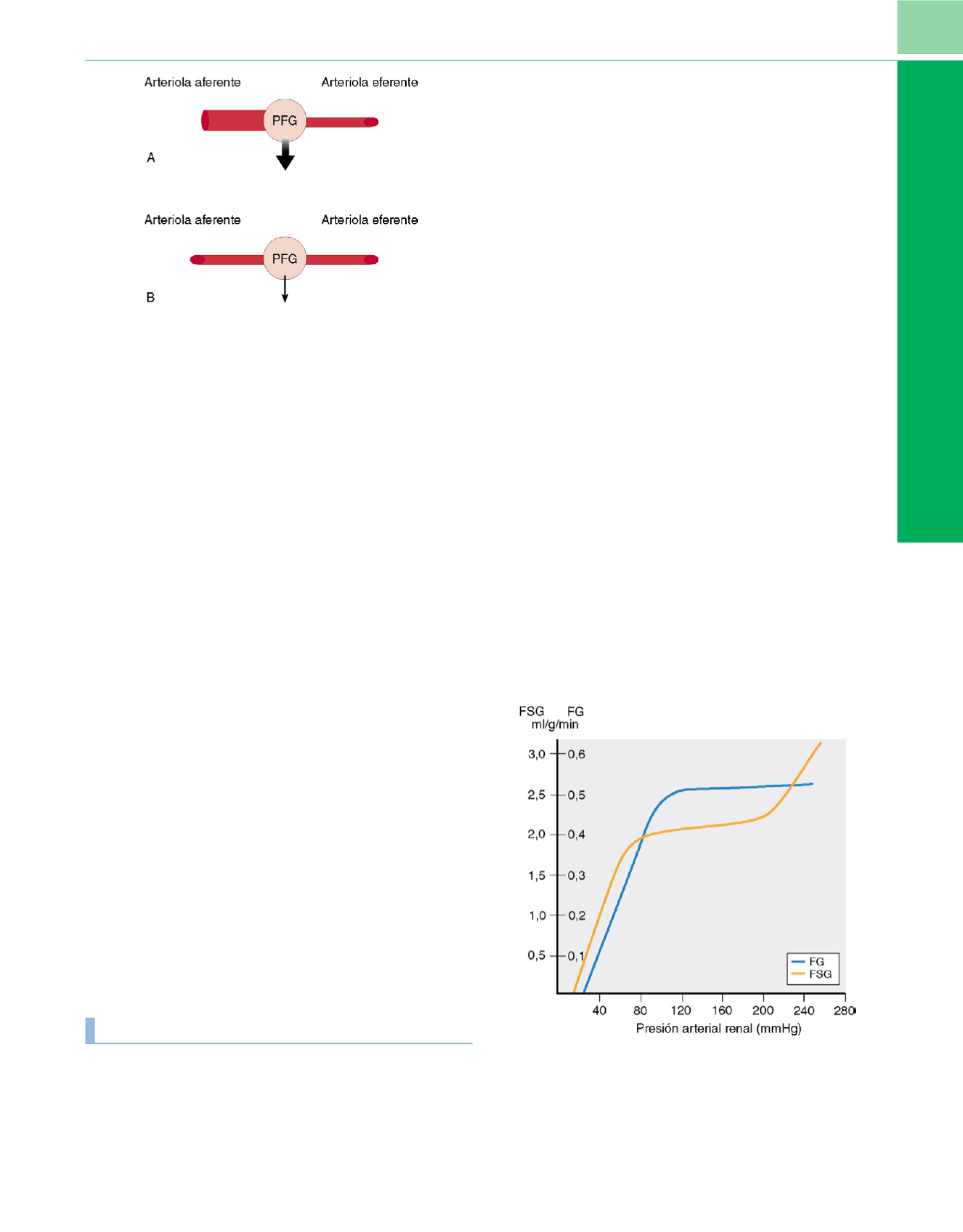
Figura 8-4
Mecanismos de control arteriolar aferente y eferente. PFG,
presión de filtración glomerular.
(De Sladen RN, Landry D: Renal blood flow
regulation, autoregulation, and vasomotor nephropathy.
Anesthesiol Clin
North Am
18:791-807, ix, 2000.)









