
El túbulo proximal es también un lugar destacado de secre-
ción de muchos aniones endógenos (sales biliares, urato), cationes
(creatinina, dopamina) y fármacos (diuréticos, penicilina, probe-
necid, cimetidina). Los iones orgánicos compiten entre sí por los
sistemas de transporte de proteínas. Por tanto, la administración
de probenecid altera la secreción tubular de penicilina y prolonga
su acción. En la insuficiencia renal crónica, los ácidos orgánicos se
acumulan y compiten con los fármacos como la furosemida por las
proteínas secretoras, por lo que producen una aparente «resisten-
cia» a los diuréticos de asa.
Asa gruesa ascendente de Henle
Éste es el componente activo, desde el punto de vista metabólico,
del asa de Henle que reabsorbe alrededor del 20% del sodio, cloruro,
potasio y bicarbonato filtrados. Sólo el asa descendente es permea-
ble al agua. En el asa gruesa ascendente impermeable al agua, el
sodio se reabsorbe de forma activa, pero el agua permanece. En
este llamado segmento dilutor del riñón, el líquido tubular dismi-
nuye su osmolalidad a menos de 150mOsm/kg H
2
O.
Al igual que en el túbulo proximal, la bomba Na
+
-K
+
-ATPasa
de la membrana basolateral es el motor que dirige la capacidad reab-
sortiva del asa gruesa ascendent
e 12 .El sodio se desplaza desde la luz
tubular por difusión pasiva a lo largo de su gradiente de concentra-
ción. Un sistema de antiporte Na
+
/H
+
de la membrana celular apical
media la secreción neta de H
+
y la reabsorción de bicarbonato.
Un destacado sistema de proteínas de simporte acopla la
reabsorción de sodio, cloruro y potasio (el último en contra de su
gradiente de concentración) a través de la membrana apical. El
bloqueo de este sistema es el principal mecanismo de acción de los
diuréticos de asa a la hora de inhibir la reabsorción de NaCl en el
asa gruesa ascendente de Henle.
Equilibrio de oxígeno en el asa gruesa
ascendente medular
Los riñones reciben el 20% del gasto cardíaco total, pero extraen
relativamente poco oxígeno. La diferencia arteriovenosa renal de
oxígeno [(a – v)O
2
] es de sólo 1,5ml/dl. Sin embargo, existe una
marcada discrepancia entre la corteza y la médula renales respecto
al flujo sanguíneo y al aporte y consumo de oxígeno
( fig. 8-9y
tabla 8-1 ). La médula recibe sólo el 6% del FSR y tiene una presión
media de oxígeno (Po
2
) de 8 mmHg. Por tanto, resulta posible que
se desarrolle una hipoxia intensa en la médula a pesar de que el
FSR total sea adecuado de forma relativa. El asa gruesa ascendente
medular de Henle, de activo metabolismo, es muy vulnerable
13 .Este segmento es también susceptible de lesión nefrotóxica.
El flujo sanguíneo intrarrenal está regulado por compuestos vaso-
activos endógenos. En la corteza externa, a diferencia de su efecto
vasoconstrictor en otros lugares, la adenosina induce vasoconstric-
ción a través de la estimulación del receptor A
1
de la adenosina. En
la zona yuxtamedular profunda, las prostaglandinas endógenas y
el óxido nítrico estimulan la vasodilatación. El efecto neto es dirigir
todo el flujo sanguíneo disponible hacia la médula. Los fármacos
que inhiben la síntesis de prostaglandinas, como los antiinflamato-
rios no esteroideos (AINE), pueden alterar este mecanismo com-
pensador y producir isquemia medular.
El estrés (dolor, traumatismo, hemorragia, hipoperfusión,
sepsis, insuficiencia cardíaca congestiva) activa el sistema simpáti-
co-suprarrenal y produce una vasoconstricción cortical renal y una
posible isquemia tubular. El riñón está relativamente desprovisto
de receptores
b
2
, de forma que la liberación de adrenalina induce
sobre todo vasoconstricción mediada por receptores
a
o por la
activación de angiotensina.
Fisiología renal
215
8
Sección I
Fisiología y anestesia
© ELSEVIER. Fotocopiar sin autorización es un delito
Tabla 8-1
Distribución del flujo sanguíneo renal entre la corteza y la médula
Corteza
Médula
Porcentaje del flujo sanguíneo renal
94
6
Flujo sanguíneo (ml/min/g)
5,0
0,03
P
o
2
(mmHg)
50
8
Proporción de extracción de O
2
(V
o
2
/D
o
2
)
0,18
0,79
La médula renal recibe únicamente una pequeña fracción del flujo sanguíneo renal
total, y sus flujos son muy lentos. Como resultado, la presión de oxígeno tisular es
muy baja y la médula extrae casi el 80% del oxígeno que se le suministra, por lo que
una mínima reducción de los flujos sanguíneos renales total y cortical puede inducir
isquemia e hipoxia en la médula renal.
D
o
2
, aporte de oxígeno; P
o
2
, presión de oxígeno; V
o
2
, consumo de oxígeno.
Datos de Brezis M y cols.: The pathophysiological implications of medullary hypoxia.
Am J Kidney Dis
13:253-258, 1989.
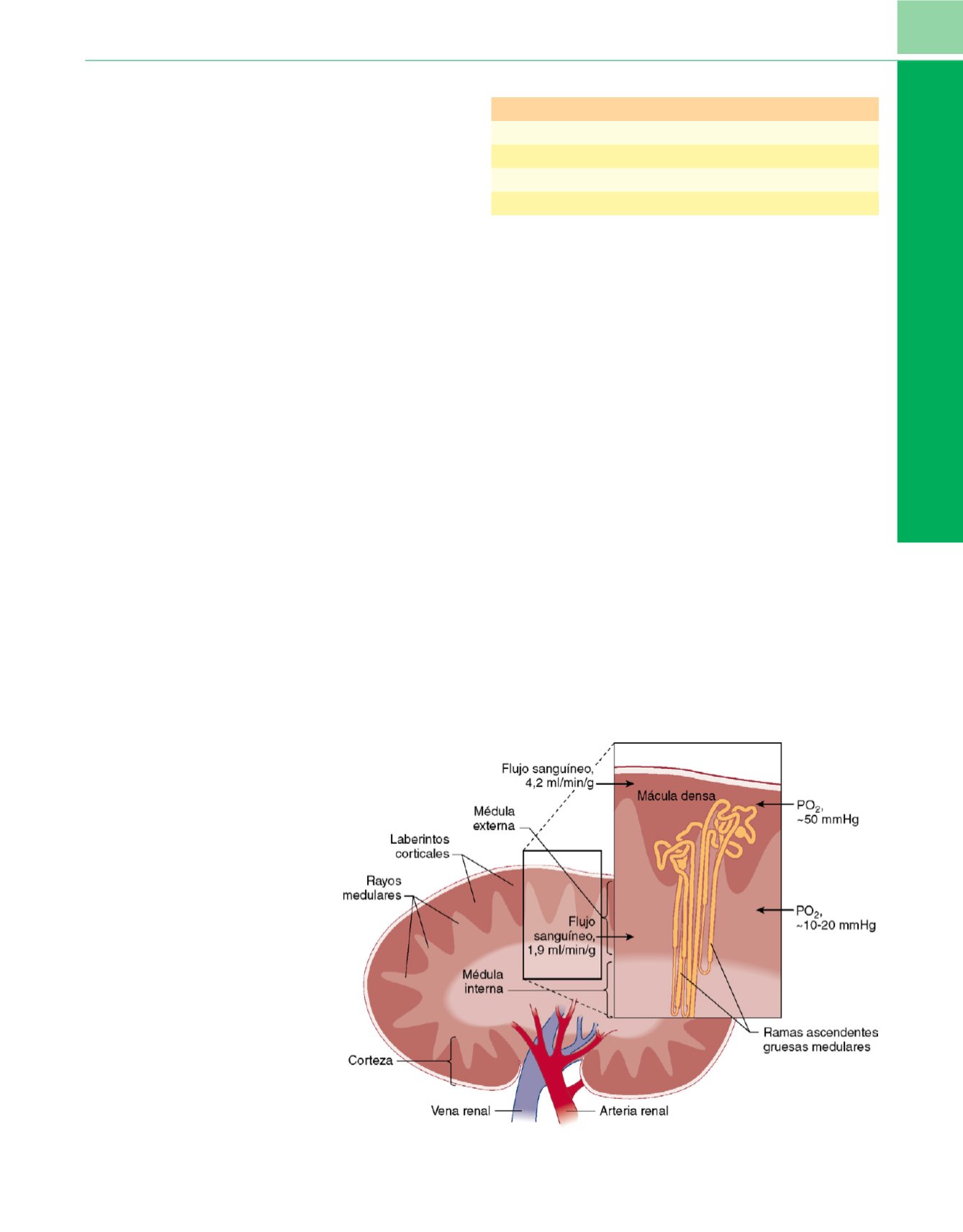
Figura 8-9
Hipoperfusión medular. Para
generar y mantener el intercambio
contracorriente que proporciona la capacidad
de concentrar la orina, el flujo sanguíneo
medular debe ser lento. Las zonas
yuxtamedular y medular son zonas de bajo
flujo sanguíneo e hipoxia tisular relativa. Los
componentes de la nefrona que tienen alto
consumo de oxígeno como la rama gruesa
ascendente medular (RGAm) tienen alto riesgo
de desequilibrio entre la oferta y demanda de
oxígeno y lesión isquémica.
(De Brezis M,
Rosen S: Hypoxia of the renal medulla—its
implications for disease.
N Engl J Med
332:647-655, 1995.)









