
tras la cirugía, en lugar de una insuficiencia renal que requiera
diálisis; la alteración de la filtración máxima se compara con un
umbral crítico o con la función renal basal. Aunque la mayoría de
los marcadores de alteración de la filtración renal basados en
la creatinina sérica se han validado mediante su asociación con la
mortalidad postoperatoria, hay poco consenso sobre una modali-
dad de evaluación estánda
r 129; en una revisión de 28 estudios perio-
peratorios controlados no se encontraron dos de ellos que tuviesen
los mismos criterios de LRA o IR
A 23. Muchos estudios presentan
una variedad de marcadores de LRA para describir un efect
o 130.
La función renal se monitoriza de forma indirecta. Entre las
causas obstructivas que pueden iniciar la LRA, se debe descartar
una oclusión o acodamiento de la sonda urinaria como causa de
oliguria. Entre las causas tóxicas de LRA hay que citar los antibió-
ticos (p. ej., aminoglucósidos, anfotericina B) o los contrastes
radiológicos. Por ejemplo, con los aminoglucósidos, la nefrotoxi-
cidad se correlaciona poco con las concentraciones en el tejido
renal o plasmáticas del fármaco, pero aumenta de forma conside-
rable por la presencia simultánea de depleción de volumen o de
cirrosis hepátic
a 20 .Por el contrario, la probabilidad de LRA se
correlaciona con la alteración renal basal y con la cantidad de
contraste radiológico inyectado, sobre todo cuando la proporción
entre el volumen de contraste y el aclaramiento de creatinina es
mayor de
6 131 .La vigilancia del anestesiólogo es el primer elemento
de monitorización necesario para conservar la función renal.
La monitorización de la función renal que puede efectuarse
durante el período perioperatorio se relaciona en gran medida con
la programación cronológica perioperatoria, el destino postopera-
torio del paciente y el procedimiento quirúrgico. A diferencia del
contexto postoperatorio/cuidados intensivos, donde la monitoriza-
ción de la función renal puede implicar la evaluación periódica de
dicha función en unas condiciones relativamente estables, la moni-
torización renal intraoperatoria implica un período más breve y más
inestable, en el que suele haber una pérdida de sangre significativa,
desplazamientos considerables de líquidos, amplias fluctuaciones
hemodinámicas e incluso un compromiso directo del flujo sanguí-
neo de la arteria renal; todos estos factores socavan el equilibrio
estacionario tan esencial para la mayoría de las pruebas estándar de
función renal, como el aclaramiento de creatinina. El anestesiólogo
suele confiar en variables indirectas, como el volumen de orina, para
evaluar la perfusión renal. Por desgracia, la diuresis no refleja con
fiabilidad la filtración glomerular y la función renal en las condicio-
nes intraoperatorias. Incluso el conocimiento del flujo sanguíneo de
la arteria renal no es especialmente informativo, porque el incre-
mento del flujo obliga a un aumento de la filtración y demandas de
transporte activo, así como a un mayor aporte de oxígeno. Como se
ha descrito con anterioridad, un parámetro de monitorización del
equilibrio entre el aporte y la demanda de perfusión renal regional,
sobre todo en la médula renal, sería una herramienta de monitori-
zación directa ideal, aunque en la actualidad no está disponible. Las
mejores herramientas de las que se dispone en este momento de
forma intraoperatoria son parámetros de monitorización hemodi-
námica indirecta que pueden ayudar a optimizar las condiciones
compatibles con el bienestar renal, como asegurar unos niveles ade-
cuados de volumen intravascular (es decir, precarga), rendimiento
cardíaco y perfusión sistémica. Los índices de bioquímica sérica y
urinarios pueden permitir la evaluación de una distribución ade-
cuada del gasto cardíaco a los propios riñones.
Marcadores indirectos
de una perfusión y función
renales óptimas
Los estudios epidemiológicos no quirúrgicos muestran un patrón
para el desarrollo de insuficiencia renal que suele implicar la combi-
nación de deshidratación grave con enfermedades renales crónicas.
Por ejemplo, la combinación de diabetes mellitus y depleción de
volumen incrementa la probabilidad de desarrollar IRA en 100 vece
s 20 .Los métodos preoperatorios más prácticos para evaluar la volemia
son la anamnesis preoperatoria estándar y la exploración física, así
como la evaluación de los cambios de presión arterial en respuesta a
las condiciones cambiantes. Un paciente despierto no suele tener
cambios ortostáticos significativos de presión arterial a menos que
esté deshidratado, mientras que un paciente anestesiado y con un
grado similar de deshidratación puede presentar cambios paradójicos
del pulso arterial con la inspiración con presión positiv
a 132.
Aporte de oxígeno: gases sanguíneos,
equilibrio acidobásico y hematocrito
Una hipoxemia arterial grave que llegue a una presión parcial arte-
rial de oxígeno (Pao
2
) menor de 40 mmHg se asocia a una dismi-
nución del FSR y a vasoconstricción rena
l 133,134 .Parece que la hipoxia
sistémica puede producir antidiuresis y natriuresis con independen-
cia de la inervación rena
l 135. La capnometría puede ser un elemento
de monitorización útil, porque la hipercapnia se ha asociado con
una disminución del FSR en pacientes que requieren ventilación
mecánic
a 136. Los estudios realizados en animales indican que las
desigualdades de demanda de aporte de oxígeno son exageradas y
que la hipoxia medular es extrema durante la CEC, efectos que
duran mucho más allá de la separación del soporte circulatori
o 137.
Los efectos de la anemia sobre el riñón se han estudiado
sobre todo en el contexto del control de la CEC. Cuando se utilizan
soluciones de cristaloides/coloides para cebar un circuito extracor-
póreo, el inicio de la CEC obliga a una disminución de alrededor
del 30% de la capacidad de transporte de oxígeno. Los estudios en
animales respaldan que una hemodilución moderada (hematocrito
del 20-30%) es renoprotectora durante la CEC debido a la reduc-
ción de la viscosidad sanguínea y a la mejora del flujo sanguíneo
regiona
l 138,139 .Sin embargo, aunque valores de hematocrito menores
1220
Control de la anestesia
III
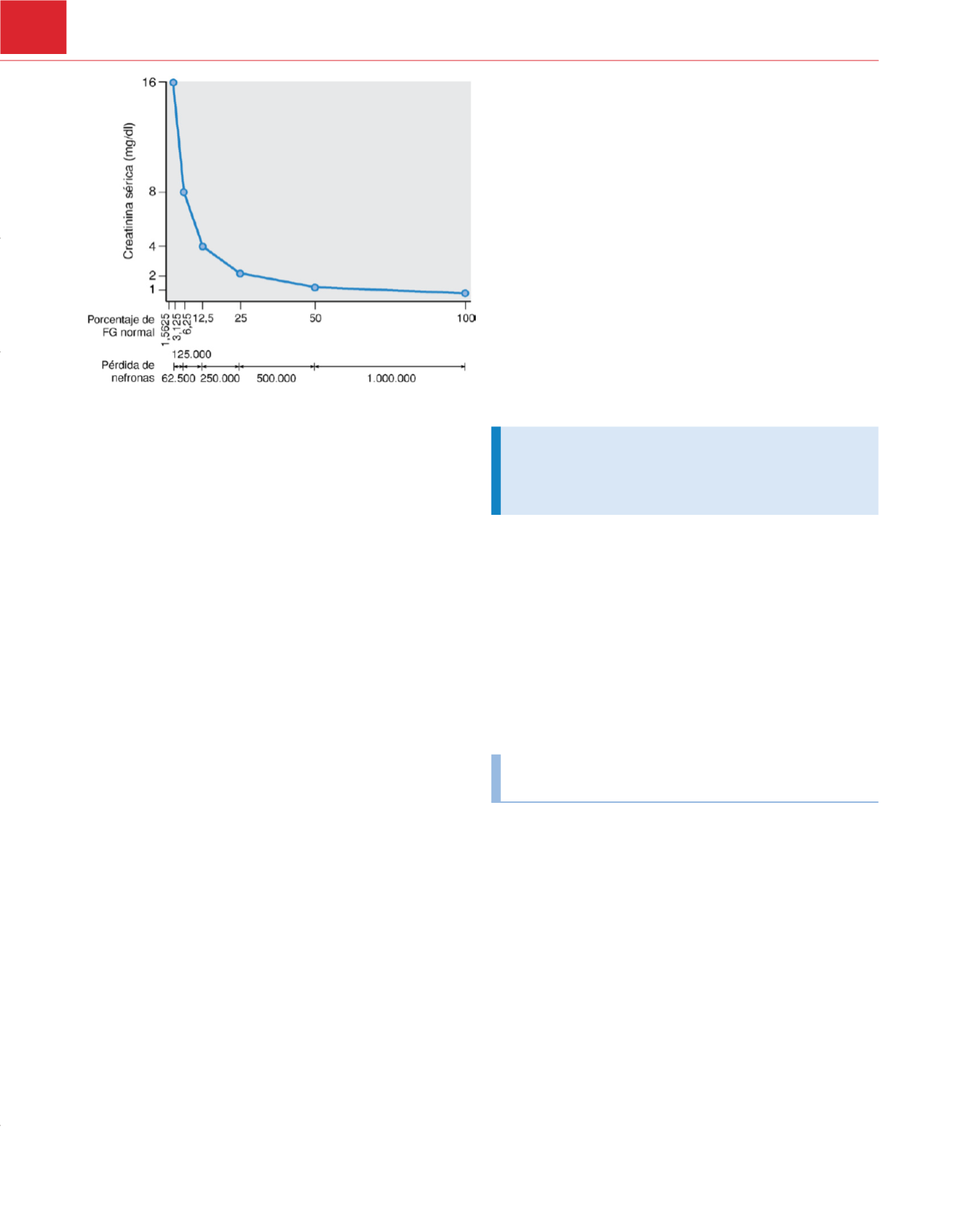
Figura 35-10
Relación logarítmica inversa entre la concentración sérica de
creatinina (eje
y
) y las reducciones relativas de filtrado glomerular (FG) y la pérdida
aproximada de nefronas (eje
x
). La relación no lineal significa que la concentración
de creatinina sérica no aumenta de forma marcada hasta que existe una
reducción del 75% del FG (p. ej., de 120 a 30ml/min).
(Modificada de Faber MD,
Kupin WL, Krishna G, Nairns RG: The differential diagnosis of ARF
. En
Lazarus JM,
Brenner BM [eds.]:
ARF,
3.
a
ed. Nueva York, Churchill Livingstone, 1993, pág. 133.)









