
multiorgánica, aumento de la utilización de recursos, un coste elevado
y un aumento de la mortalidad (v. caps. 50 y 52
) 2-10. Cada año, 1 millón
de pacientes en todo el mundo se someten a revascularización coro-
naria con CEC y alrededor de 77.000 pacientes anuales desarrollan
una LRA postoperatoria, entre los que unos 14.000 requieren diálisis
por primera ve
z 4. El mecanismo de la LRA perioperatoria durante la
cirugía cardíaca parece ser multifactorial, con la participación de fac-
tores de riesgo pre e intraoperatorios, como la disfunción renal pre-
existente,diabetes,disfunciónventricular,edadavanzada,hipertensión,
procesos micro y macroembólicos, mediadores inflamatorios, dura-
ción prolongada de la CEC, sensibilidad a la estimulación simpática,
alteración de la resistencia y flujo vasculorrenale
s 3,8,113 ,y subtipo de
hipertensión (es decir, hipertensión de la presión diferencial
) 2 .La relevancia de la CEC se ha evaluado en muchos estudios de
LRA postoperatoria en pacientes sometidos a cirugías de revasculari-
zación con y sin CE
C 114-124 ,sin que haya habido evidencias concluyen-
tes de que la CEC contribuya de forma directa a la LRApostoperatoria.
En un estudio multicéntrico reciente de pacientes sometidos a cirugía
cardíaca, los factores independientes y significativos de LRA fueron
la edad mayor de 75 años, la insuficiencia cardíaca congestiva preo-
peratoria, los antecedentes de infarto de miocardio, la enfermedad
renal preexistente, el uso intraoperatorio de múltiples inotrópicos, la
inserción intraoperatoria de un balón de contrapulsación intraaórtica
y la duración prolongada de la CEC (más de 2 horas). Además, la
presión diferencial preoperatoria (sistólica menos diastólica) mayor
de 40 mmHg tenía una relación incremental y progresiva con el riesgo
renal, de modo que por cada 20 mmHg adicionales de dicha presión
se sumaba un cociente de verosimilitudes
(odds ratio)
de 1,49 (IC
1,17-1,89;
P
=0,001). En este amplio estudio, con una elevada inciden-
cia de LRA (4,8%) tanto en las cohortes de derivación (n=2.381)
como de validación (n=2.402), la LRA era casi el doble y la mortali-
dad relacionada con factores renales el triple más frecuente en los
pacientes con una presión diferencial mayor de 80 mmHg.
Las variantes genéticas son un factor predictivo establecido
de enfermedad renal crónica (p. ej., nefropatía por trasplante renal)
y explican una variación 2-3 veces mayor de la LRA postoperatoria
que los factores de riesgo clínicos estándar por sí solo
s 125,126 .Se ha
estudiado una serie de polimorfismos candidatos de los que se sabe
que afectan a la inflamación y la vasoconstricción, y varios han
mostrado unas asociaciones firmes con la LRA poscirugía car-
díac
a 126,127 .Los hallazgos genéticos más relevantes desde el punto
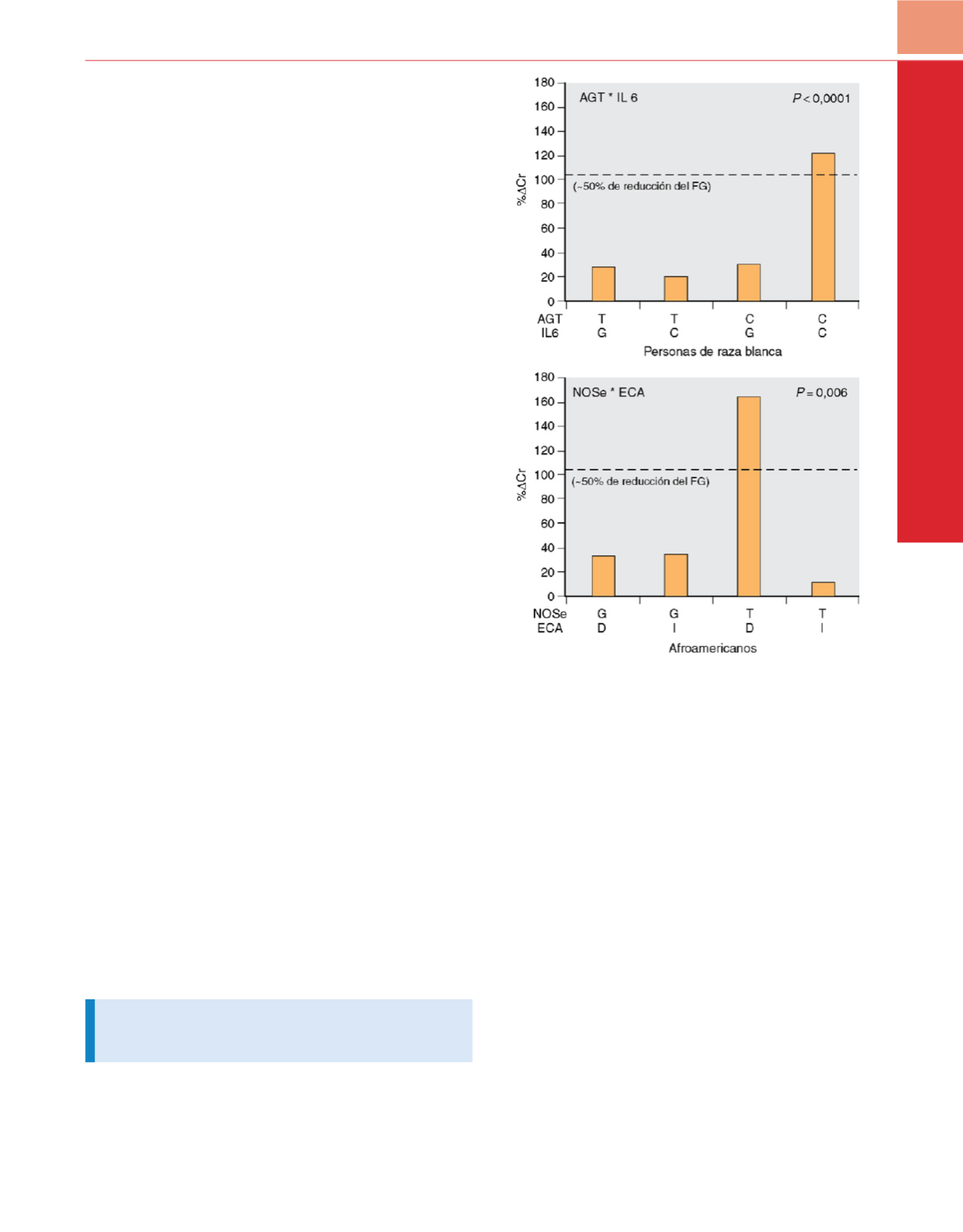
de vista clínico hasta el momento identifican la coposesión de los
polimorfismos IL-6 572C y angiotensinógeno (AGT) 842C en per-
sonas de raza blanca (9% de los pacientes) como factor predictivo
de una elevación máxima de creatinina unas 4 veces superior a la
media tras la revascularización coronaria (121%)
( fig. 35-9 )y
pueden ser viables como herramienta de detección selectiva preo-
peratoria si se validan en otras poblaciones. En personas afroame-
ricanas, un hallazgo similar, pero con menos potencia estadística,
es la coposesión de los polimorfismos de la oxidonitricosintasa
endotelial (NOSe) 894T y la deleción de la enzima convertidora de
angiotensina, que también predicen un gran aumento de creatinina
(162,5%) (v.
fig. 35-9 ). Esta evidencia convincente de una base
genética para la LRA postoperatoria proviene del análisis de un
número relativamente pequeño de variantes genéticas candidatas.
Parámetros de monitorización
de la función renal
En pacientes con LRA perioperatoria, una de las principales difi-
cultades para lograr un tratamiento perioperatorio óptimo y una
intervención precoz ha sido la ausencia de herramientas para reco-
nocer de forma precoz una LRA sutil. Las herramientas tradicio-
nales de monitorización de la insuficiencia renal suelen ser
insensibles hasta que quedan menos del 40% de nefronas funcio-
nales normales
( fig. 35-10); esto deja sólo un pequeño margen de
función renal antes de que aparezcan síntomas urémicos, cuando
quedan menos del 5% de nefronas funcionales normale
s 58 .El máximo estándar para demostrar la conservación renal
perioperatoria es la evitación de tratamiento de sustitución renal y
la reducción de la mortalidad. Por ejemplo, el tratamiento post
operatorio óptimo de la hiperglucemia en pacientes en estado crítico
reduce la incidencia de diálisis y mejora la supervivenci
a 128 .Por
desgracia, la mayoría de los estudios no tienen un tamaño muestral
suficiente para demostrar diferencias de la mortalidad o en las tasas
de diálisis y en su lugar se utilizan sustitutos.
En la mayoría de las ocasiones, la conservación renal se mide
utilizando criterios de valoración sustitutos secundarios como mar-
cadores de diálisis y mortalidad. Las mediciones secundarias refle-
jan en la mayoría de los casos cambios de la filtración glomerular
Monitorización de la función renal
1219
35
Sección III
Control de la anestesia
© ELSEVIER. Fotocopiar sin autorización es un delito
Figura 35-9
La LRA tras la cirugía cardíaca se predice mejor conociendo las
variantes genéticas que sólo con los factores de riesgo clínicos estándar.
Las combinaciones habituales de polimorfismo genético predicen un mayor
riesgo; angiotensinógeno (AGT) 842T
→
C e interleucina (IL) –6 572G
→
C en
personas de raza blanca; óxido nítrico sintasa endotelial (NOSe) 894G
→
T y enzima
convertidora de angiotensina (ECA) inserción/deleción (I/D) en afroamericanos.
%
∆
Cr, máximo aumento sérico fraccionado de creatinina; FG, filtrado glomerular.
(Con autorización de Stafford-Smith M, Podgoreanu M, Swaminathan M y cols.:
Association of genetic polymorphisms with risk of renal injury after coronary
artery bypass graft surgery
. Am J Kidney Dis
45:519-530, 2005.)









