
(una menor Po
2
venosa acelera la difusión desde el comienzo). Las
membranas alveolocapilares engrosadas prolongarán el proceso de
equilibrado, con la posible consecuencia de producir hipoxemia.
También se debe mencionar que la mayor parte del oxígeno
que se disuelve en el plasma difunde hacia los eritrocitos y se une
a la hemoglobina. Un gramo de hemoglobina se puede unir a
1,36ml de O
2
(se utilizan cifras entre 1,34 y 1,39). Esto significa
que 1 l de sangre con un contenido de hemoglobina de 150 g/l se
puede unir a 204ml de O
2
cuando está saturada por completo. Con
una saturación del 98%, que es la que se consigue normalmente en
la sangre arterial, el oxígeno unido a la hemoglobina equivale a
200ml/l de sangre. Esto se debe comparar con la cifra de tan sólo
3ml de O
2
que está disuelto físicamente en 1 l de sangre a una Pao
2
de 100 mmHg (13,3 kPa). El oxígeno unido a la hemoglobina no
crea presión en el plasma, lo que es importante porque permite que
mucho más oxígeno difunda a través de las membranas antes de
que se alcance un equilibrio de presiones. La anemia reduce la
capacidad de difusión, y la policitemia la incrementa.
P
eso
molecular
. La difusión se relaciona inversamente
con la raíz cuadrada del peso molecular del gas. Así, cuanto mayor
sea la molécula, mayor dificultad tendrá para atravesar las mem-
branas. El O
2
es un gas relativamente ligero, con un peso molecular
de 32. El CO
2
es más pesado, con un peso molecular de 44, por lo
que debería tener una difusión menor que el O
2
. Sin embargo, la
obtención de la raíz cuadrada del peso reduce la diferencia entre
los gases, y en la práctica el CO
2
es mucho más difusible que el O
2
,
como se explica en el párrafo siguiente.
S
olubilidad
. La difusión se relaciona linealmente con la
solubilidad en los tejidos. Normalmente, se toma como referencia
la solubilidad del agua. El CO
2
es casi 30 veces más soluble en agua que
el O
2
y difunde a una velocidad más de 20 veces mayor (el efecto neto
de todos los factores ya mencionados
) 31 .En la práctica esto significa
que no hay ninguna enfermedad pulmonar compatible con la vida que
produzca un deterioro mensurable de la difusión del CO
2
.
Perfusión pulmonar
Relación presión-flujo
Al contrario de la circulación sistémica, la circulación pulmonar es un
sistema de baja presión. La presión típica en la arteria pulmonar de
20 mmHg de sistólica y 8 mmHg de diastólica es aproximadamente
6-10 veces menor que la presión en las arterias sistémicas. La menor
presión se consigue por el mayor diámetro vascular y por la menor lon
gitud de los vasos pulmonares en relación con los sistémicos. En
particular, una luz vascular grande reduce la necesidad de presión
impulsora. Según la ley de Poiseuille, un aumento del radio vascular
reduce la necesidad de presión en un exponente de 4 para mantener un
flujo determinado, si el flujo es lineal. Con el flujo turbulento la depen-
dencia de las dimensiones vasculares será aún mayor. Como conse-
cuencia de la menor resistencia, el flujo sanguíneo capilar pulmonar es
pulsátil,al contrario del flujo continuo en los capilares sistémico
s 33 .Otra
consecuencia probablemente más importante de la baja presión es que
las paredes capilar y alveolar pueden ser muy delgadas sin que se pro-
duzca escape de plasma, lo que facilita la difusión del O
2
y del CO
2
. Un
aumento súbito de la presión arterial pulmonar hasta por encima de
una media de 30 mmHg produce trasudación del plasma hacia los
espacios intersticial y alveolar, lo que da lugar a la formación de edema
pulmonar.Un aumentomás lento de la presión,en un período demeses
o años, estimula el crecimiento del músculo liso vascular («remodelado
vascular»), con engrosamiento de la pared vascula
r 34 .El edema se pre-
viene mejor, a pesar de una hipertensión pulmonar incluso grave, pero
habrá deterioro de la capacidad de difusión.
Distribución del flujo sanguíneo pulmonar
El flujo sanguíneo pulmonar está gobernado por la presión impul-
sora y la resistencia vascular. Si estos factores están distribuidos de
forma heterogénea, la perfusión también puede ser heterogénea.
Parece que éste es el caso. En los últimos años ha habido interés en
la distribución de la perfusión y los mecanismos subyacentes a la
misma. Así, la explicación general y previamente aceptada de una
orientación gravitacional de la perfusión, como se demostró en el
trabajo pionero de Permutt, West, Hughes y otros autores (v. una
revisión en la referencia 35), ha sido puesta en duda por otros autores
que proponen una distribución «fractal» donde la gravedad tiene
una participación pequeñ
a 36 .Aquí abordaremos primero el concepto
«gravitacional» y después pasaremos al concepto «fractal».
Distribución gravitacional del flujo sanguíneo pulmonar
La presión arterial pulmonar aumenta hacia las partes inferiores del
pulmón, como efecto de la presión hidrostática que se acumula en el
recorrido desde la parte superior hasta la inferior del pulmón. Esta
presión aumenta 1cmH
2
O/cm de distancia hacia la parte inferior del
pulmón (o 0,74mmHg/cm de distancia vertical; la sangre tiene una
densidad próxima a 1, o 1,04). Esto produce una diferencia de presión
en los vasos arteriales pulmonares entre el vértice y la base de
11-15 mmHg, dependiendo de la altura del pulmón. De esta manera,
hay menos fuerza impulsora hacia el vértice pulmonar. Como la
presión arterial pulmonar media es de aproximadamente 12 mmHg
al nivel del corazón, puede ser cercana a cero en el vértice pulmonar
en bipedestación. Además, si aumenta la presión alveolar, como
durante la ventilación con presión positiva, puede superar a la de la
arteria pulmonar y comprimir los capilares pulmonares. En ese caso
no fluirá sangre a través de los vasos.Esa parte del pulmón se denomina
zona I, de acuerdo con la nomenclatura introducida por West y cols.
( fig. 5-11 ) 35 .Si la presión arterial y la presión capilar superan a la
presión alveolar, como ocurre en zonas más inferiores del pulmón
como consecuencia de la adición de la presión hidrostática, se esta-
blecerá un flujo sanguíneo. La presión de perfusión será la presión
arterial menos la presión alveolar, siempre que esta última presión su
pere a la de las venas pulmonares. Esto difiere de lo que ocurre en
Fisiología respiratoria
137
5
Sección I
Fisiología y anestesia
© ELSEVIER. Fotocopiar sin autorización es un delito
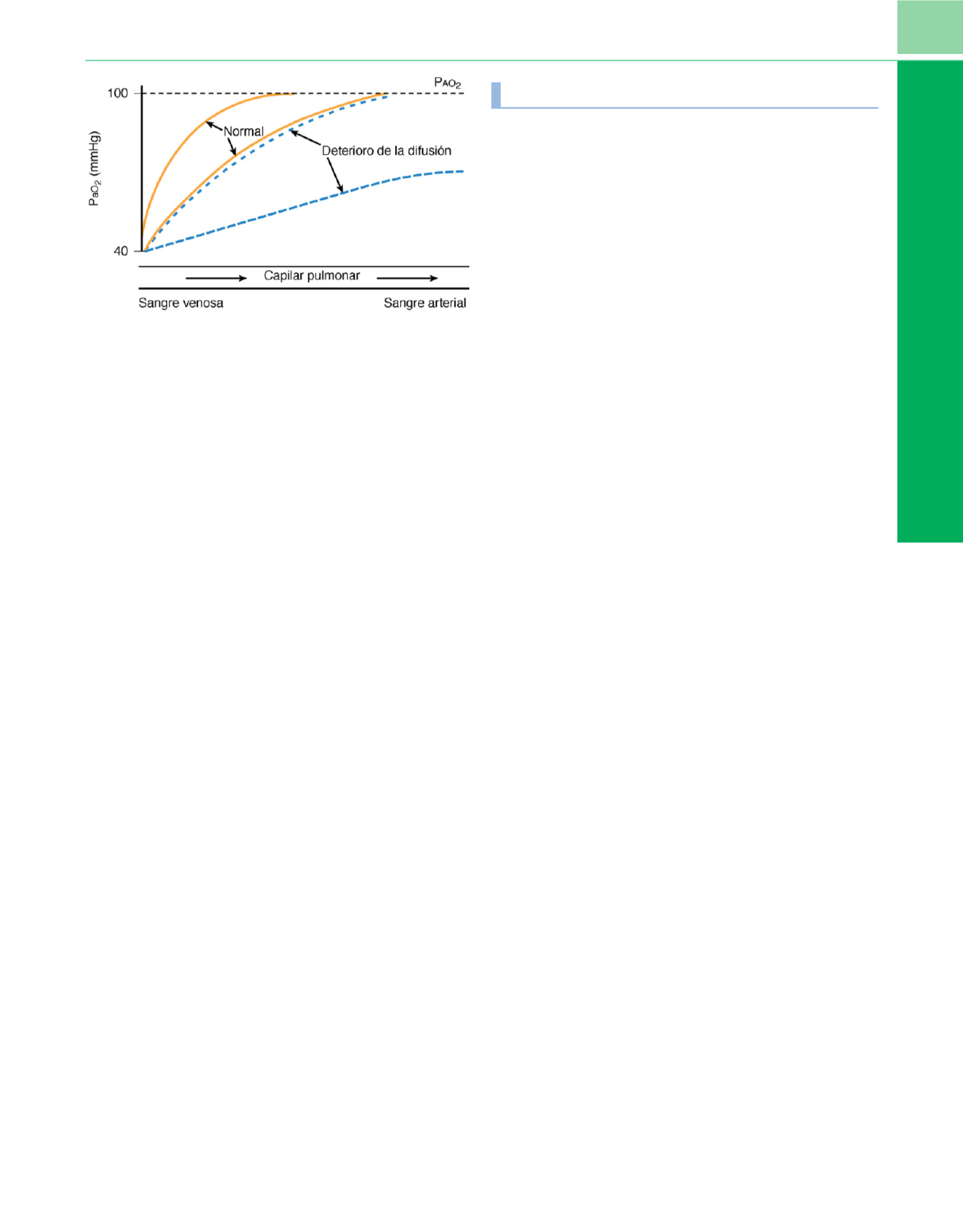
Figura 5-10
Oxigenación de la sangre capilar pulmonar en reposo y durante
el ejercicio en una persona normal y en un paciente con una neumopatía
fibrótica con deterioro de la difusión. En una persona normal el equilibrio de
la presión parcial de oxígeno en la sangre capilar con la del gas alveolar es
rápido. Esto se ha conseguido en un tercio de la distancia capilar. Sin
embargo, durante el ejercicio hay que utilizar la mayor parte de la distancia
capilar para alcanzar el equilibrio entre la presión parcial de oxígeno alveolar
y capilar pulmonar. Esto es un efecto del menor tiempo de tránsito de los
eritrocitos que produce el aumento del gasto cardíaco. La distensión y el
reclutamiento de los capilares pulmonares pueden compensar en cierta
medida el efecto del aumento del gasto cardíaco sobre la velocidad de la
sangre a través de los capilares. Cuando hay deterioro de la difusión, el
equilibrio tarda más en alcanzarse, pero a pesar de todo se puede conseguir
un equilibrio completo en reposo. Sin embargo, con el aumento de la
velocidad de la sangre durante el ejercicio el equilibrio del oxígeno puede
distar mucho de ser completo al final del capilar pulmonar, lo que produce
desaturación de la sangre arterial, que en ocasiones puede ser grave.









