
en función del área del canal vertebral
( tabla 41-1). Los dos liga-
mentos amarillos se unen (fusionan) de forma variable en la línea
media, y esta fusión, o la ausencia de unión de ambos ligamentos
amarillos, se produce a alturas vertebrales distintas en cada
pacient
e 27. Justo por detrás del ligamento amarillo se encuentran
las láminas y las apófisis espinosas de los cuerpos vertebrales o los
ligamentos interespinosos. Por detrás de dichas estructuras está
el ligamento supraespinoso, que se extiende desde la protuberan
cia occipital externa hasta el cóccix, y que une las apófisis espinosas
(v.
fig. 41-4).
En ocasiones, una técnica epidural correcta en apariencia
puede seguirse de una anestesia clínicamente unilatera
l 31,32.
Hoga
n 33ha demostrado también en cadáveres que la distribución
de una solución después de una inyección epidural en el interior
de los tejidos del espacio epidural no es uniforme, y según él, era
la causa principal de la imprevisibilidad de la distribución epidural
del fármaco.
Blomber
g 34utilizó técnicas fibroópticas para demostrar que
el espacio subdural extraaracnoideo es fácilmente penetrable en el
66% de los intentos de autopsia en seres humanos. A pesar de que
es un problema clínico poco común con la anestesia epidural,
permite comprender de manera visual las complicaciones subdu-
rales de la anestesia epidura
l 35. Blomber
g 36continuó su abordaje
endoscópico para entender la anatomía neuroaxial con un estudio
subaracnoideo. En las muestras de autopsia observó que, en las
regiones torácica inferior y lumbar superior, existía una estructura
distinta en la línea media posterior. Asimismo, advirtió que en
muchas personas existían nexos fibrosos entre las raíces nerviosas
y otras estructuras subaracnoideas, y afirmó que dichas estructuras
y nexos fibrosos podrían ayudar a explicar algunas de las variacio-
nes de la anestesia raquídea.
La realización de la anestesia caudal exige unos conocimien-
tos ampliados de la anatomía epidural y, en especial, de las varia-
ciones frecuentes de la anatomía sacr
a 37 .El sacro se origina por la
fusión de las cinco vértebras sacras. El hiato sacro, que se debe a
la falta de fusión en la línea media de las láminas de S5 y en general
de parte de S4, es el detalle de interés. Esto origina un defecto óseo
en forma de V invertida con una configuración y un tamaño varia-
bles recubierto por el ligamento sacrococcígeo posterior, el equiva-
lente funcional al ligamento amarillo. Este hiato se puede identificar
localizando los cuernos sacros, vestigios de las carillas articulares
de S5
( fig. 41-5 ). Este defecto óseo permite acceder al canal sacro,
si bien la inserción de la aguja a través de dicho defecto puede
resultar difícil debido al gran número de variantes anatómicas. Así,
por ejemplo, la forma del espacio puede variar desde una hendi-
dura hasta una V invertida de base ancha, y en 1 de cada 20 pacien-
tes el defecto óseo puede estar ausente, lo que impide el abordaje
caudal
( fig. 41-6 ) 38,39.
El canal sacro contiene la porción terminal del saco dural,
que suele finalizar normalmente por encima de una línea imagina-
ria que une las espinas ilíacas posterosuperiores, o S2. Este rasgo
también tiene una gran variabilidad, de modo que la finalización
del saco dural es más baja en los niños, aunque la facilidad para
palpar el hiato sacro en éstos hace que la técnica caudal pediátrica
Anestesias raquídea, epidural y caudal
1381
41
Sección III
Control de la anestesia
© ELSEVIER. Fotocopiar sin autorización es un delito
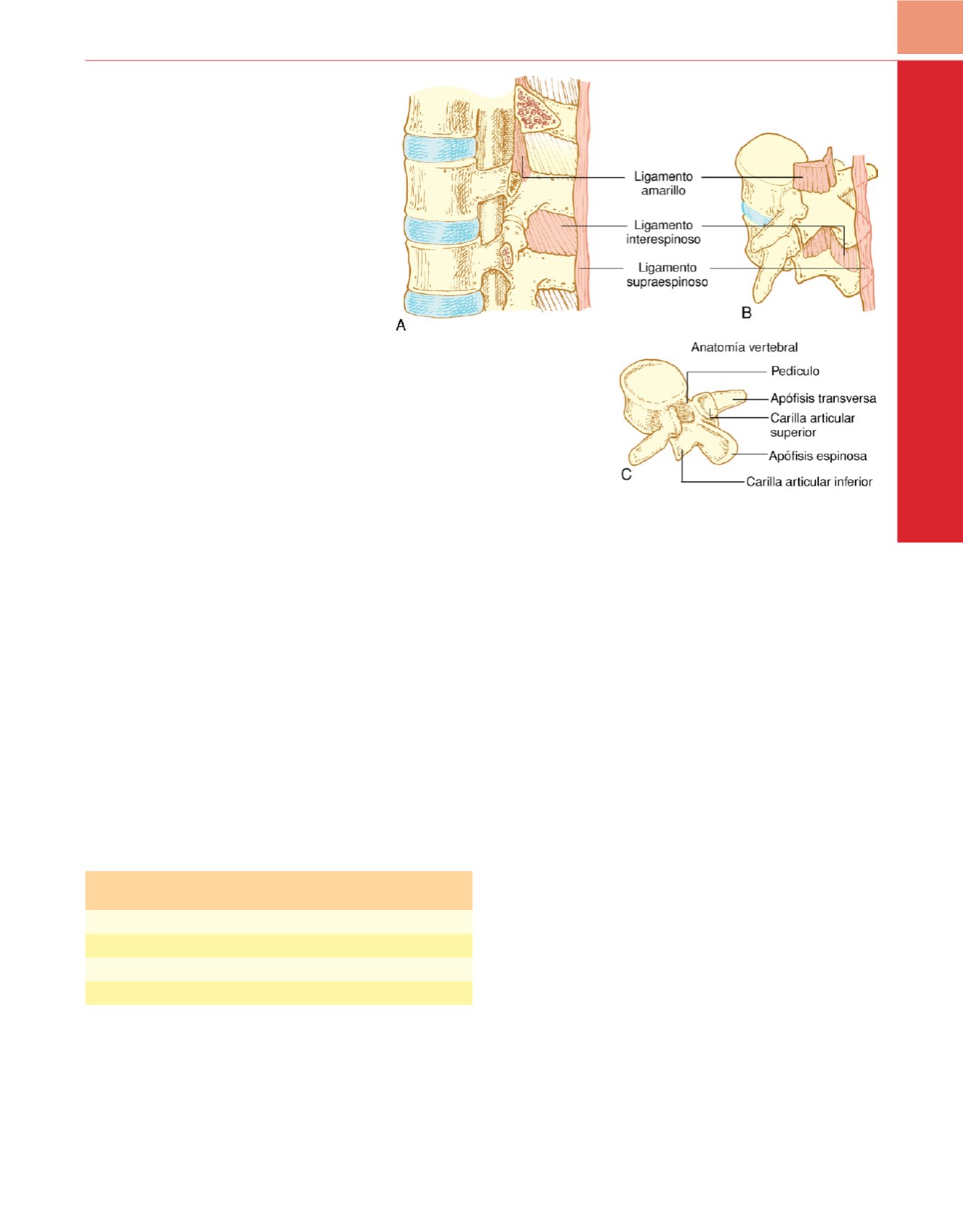
Figura 41-4
Anatomía vertebral.
A,
Proyección sagital.
B,
Proyección oblicua de las vértebras lumbares que
muestra el engrosamiento del ligamento amarillo en la
extensión caudal del espacio intervertebral y en la línea
media.
C,
Proyección oblicua de una vértebra lumbar.
Tabla 41-1
Características del ligamento amarillo a diferentes alturas vertebrales
Localización
Distancia desde la piel
al ligamento (cm)
Grosor del
ligamento (mm)
Cervical
—
1,5-3,0
Torácica
—
3,0-5,0
Lumbar
3,0-8,
0 *5,0-6,
0 †Caudal
Variable
2,0-6,0
*La distancia es de 4cm para el 50% de los pacientes y de 4-6cm para el 80% de los
pacientes.
†
Dentro de cada espacio interlaminar, el grosor del ligamento amarillo varía de
cefálico a caudal: cerca de la lámina rostral es de 1,3-1,6mm, y cerca de la lámina
caudal es de 6,9-9,1mm.
Datos de Cousins MJ, Bromage PR: Epidural neural blockade.
En
Cousins MJ, Briden-
baugh PO (eds.):
Neural Blockade in Clinical Anesthesia and Management of Pain
.
Filadelfia, JB Lippincott, 1988, pág. 255, y otras fuentes.









