
puede aumentar a más del 10% del gasto cardíac
o 217 .Durante el
período en que la aorta está pinzada transversalmente, este volumen
de sangre distiende el lado izquierdo del corazón y la vasculatura
pulmonar si la sangre no es retirada activamente. Además, los pro-
cedimientos intracardíacos introducen inherentemente aire en las
cavidades izquierdas, y este aire ha de ser retirado antes de que el
paciente se desconecte de la DCP.
Las cánulas de ventilación
(vent)
facilitan la descompresión
y la salida de aire del corazón. Lo más común es ventilar el corazón
en la raíz aórtica o directamente a partir del ventrículo izquierdo.
Los conductos de ventilación en la raíz aórtica utilizan la misma
cánula que se utiliza para liberar anterógradamente la solución
cardiopléjica y extraer sangre y aire del ventrículo izquierdo a
través de la válvula aórtica y al interior del reservorio del circuito
de CEC. Dado que la aguja de cardioplejía anterógrada es de
pequeño calibre y se posiciona por encima de la válvula aórtica, los
conductos de ventilación de la raíz tienen varias limitaciones sig-
nificativas: no pueden utilizarse cuando se está administrando la
solución cardiopléjica anterógrada y no son efectivos en la descom-
presión del ventrículo izquierdo cuando se ha retirado la pinza
transversal. Por lo general, estas limitaciones no son significativas
en el caso de un procedimiento de CDC no complicada, pero en
los pacientes sometidos a CRC con función ventricular muy com-
prometida y en todos los procedimientos intracardíacos, la venti-
lación directa del ventrículo izquierdo es esencial. Los conductos
de ventilación en el ventrículo izquierdo son introducidos típica-
mente a través de la vena pulmonar superior derecha y se avanzan
a través de la aurícula izquierda (AI), a través de la válvula mitral
al interior del ventrículo izquierdo. La cánula de 10-14 Fr utilizada
para esta finalidad ofrece una capacidad de ventilación significati-
vamente mayor que la ventilación en la raíz. Cuando sea necesario
se pueden extraer flujos de varios litros por minuto a través de estas
cánulas y al estar insertadas directamente en el interior del ventrí-
culo izquierdo, son efectivos al retirar burbujas de aire que perma-
necendespuésdehabercompletadounprocedimientointracardíaco.
Además, y dado que la ventilación del VI está separada de la cánula
de cardioplejía, puede utilizarse para descomprimir el corazón
durante la administración anterógrada de la solución cardiopléjica,
que puede requerirse en pacientes con insuficiencia aórtica. Por
desgracia, hay numerosas descripciones de casos clínicos de lesio-
nes en pacientes como consecuencia del bombeo de aire en el
corazón por un mal funcionamiento de las vías de ventilación.
Iniciación y mantenimiento de la DCP
Con el paciente coagulado y canulado puede comenzarse la DCP.
Antes de comenzar la DCP, constituye una buena práctica compro-
bar la permeabilidad de la cánula arterial. Una vez se haya confir-
mado la posición apropiada de la cánula arterial, puede comenzarse
la DCP retirando las pinzas en la línea venosa entre la cánula venosa
y el reservorio. A continuación, la sangre del paciente drena de
modo pasivo a la CEC. De modo simultáneo, la bomba arterial de
la máquina de DCP comienza a infundir la mezcla de la solución
de preparación y la sangre autóloga en el interior del paciente a
través de la cánula arterial. Es muy importante evaluar el funciona-
miento de las cánulas arteriales y venosas durante los primeros
segundos de la DCP. Debe mantenerse la presión en la vía arterial
de la CEC por debajo de 300mmHg para prevenir un traumatismo
excesivo de los elementos formes de la sangre. Se evalúa la posición
de la cánula principalmente examinando la hemodinámica del
paciente. A condición de que la cánula venosa drene adecuada-
mente el retorno venoso al corazón, la presión del lado derecho del
corazón (la PVC y la PAP) debe disminuir a 0mmHg y no obser-
varse pulso, y la presión de la sangre arterial debe alcanzar una
presión media normal (60-90mmHg) al tiempo que tampoco se
observa pulso.
La onda arterial suele llegar a no ser pulsátil a medida que
se vacía el corazón y se cambia la fuerza de bombeo desde el ven-
trículo a la bomba arterial no pulsátil de la máquina del corazón y
pulmón. Sin embargo, los pacientes con insuficiencia aórtica con-
tinúan teniendo una onda arterial pulsátil a pesar de un drenaje
venoso completo (PVC y PAP=0mmHg) por reflujo de sangre
desde la cánula arterial a través de la válvula aórtica incompetente
y devuelta al interior del ventrículo izquierdo. Si no se reduce a
cero la presión del corazón derecho, la onda arterial permanece
pulsátil y no puede aumentarse el flujo de la bomba arterial a flujo
pleno, se debe volver a evaluar la posición de las cánulas. Una vez
se haya logrado el flujo pleno, la función del corazón y del pulmón
habrá realizado completamente la transición a la máquina de DCP
y el anestesista puede desconectar el respirador.
El comienzo de la DCP se asocia con frecuencia con un
período de hipotensión, que puede ser tratado con la administra-
ción de un
a
-agonista (p. ej., fenilefrina) en el reservorio venoso
del circuito de CEC
( fig. 50-14 ). Mientras se mantiene la DCP, se
evalúa continuamente la suficiencia de la perfusión por medio de
la monitorización de las variables hemodinámicas. Se puede mani-
pular el flujo de sangre procedente de la bomba arterial en una
gama de 1,6-3,0 l/min/m
2
para liberar una presión sanguínea arte-
rial de 50-90mmHg y una saturación venosa mixta (Sv
̄
o
2
) mayor
del 65%. Cualquier hipotensión e hipertensión que se produzcan a
pesar de un flujo adecuado y Sv
̄
o
2
pueden ser tratadas ajustando
la RVS del paciente con vasoconstrictores o vasodilatadores.
Se deberán obtener muestras de gases en sangre arterial al
menos cada 30 minutos para valorar el funcionamiento del oxige-
nador y para monitorizar al paciente en relación con el desarrollo
de acidosis y un estado de anticoagulación apropiado. Unos valores
de déficit de bases de –5 o menos pueden ser corregidos con bicar-
bonato de sodio, pero en último término se deberá estudiar la causa
de base de la producción de acidosis. Puede estar indicado un
aumento del flujo y presión de perfusión. Unos valores del TCA
por debajo del parámetro institucional aceptable para la DCP (por
1682
Anestesia por subespecialidades en el adulto
IV
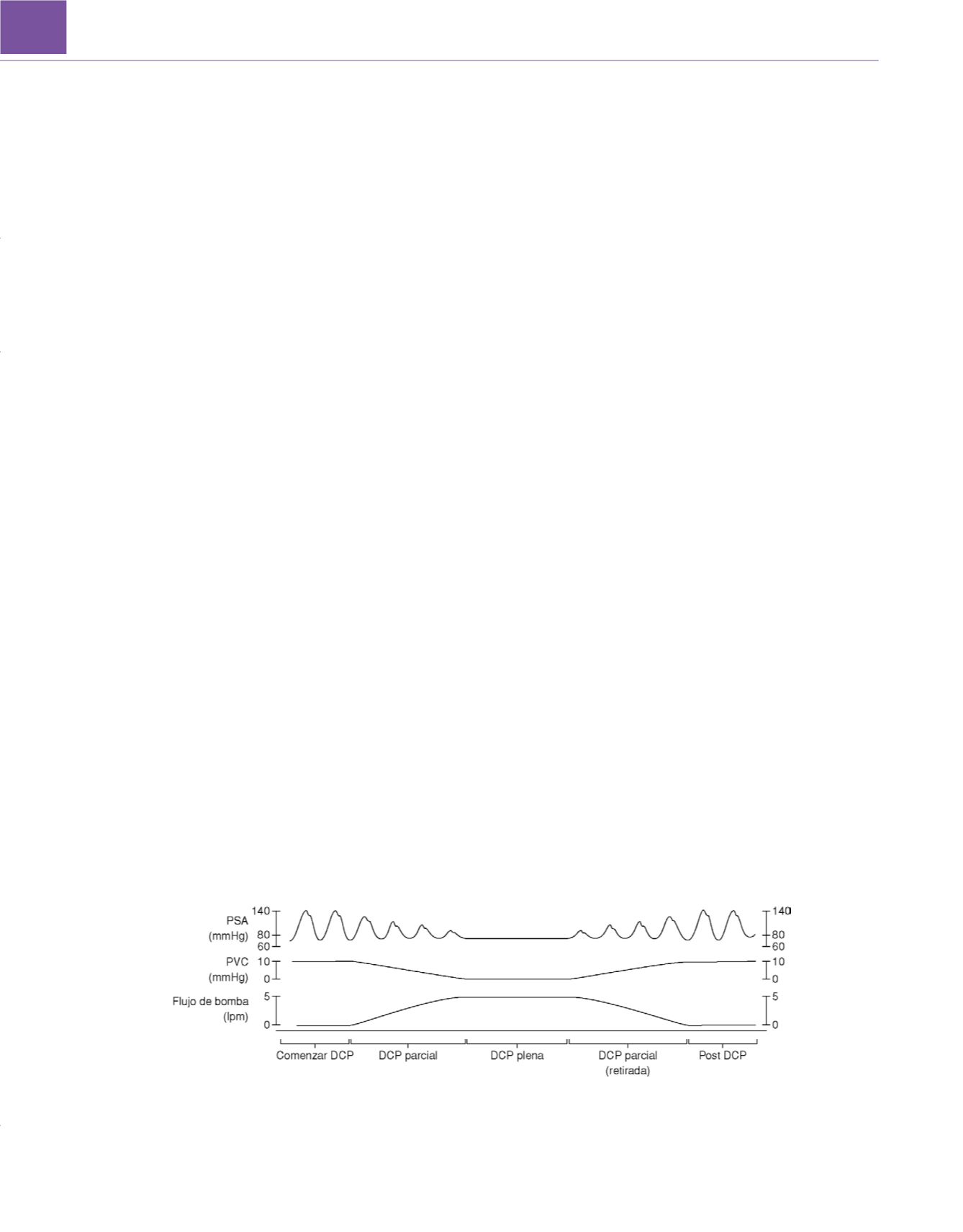
Figura 50-14
Ilustración de la hemodinámica del paciente antes de la derivación cardiopulmonar (DCP), durante el comienzo de la DCP, durante la DCP plena,
mientras se retira la DCP y después de la DCP. DCP, derivación cardiopulmonar; lpm, litros por minuto; PSA, presión sanguínea arterial; PVC, presión venosa central.









