
casos de colestasis intrahepática, depósitos excesivos de grasa y de
glucógeno y resultados elevados en las pruebas de función hepática.
Entre otros estudios metabólicos, se deben realizar de modo ruti-
nario analíticas de electrólitos, glucosa, nitrógeno ureico en sangre
y creatinina, así como de amoníaco. Con menor frecuencia, pero
también de forma regular, se han de medir los niveles de proteínas
totales, la albúmina, la hemoglobina y los triglicérido
s 214 .Pronóstico
Las probabilidades de supervivencia de un niño dependen de una
ingesta nutricional adecuada. Los lactantes con un tracto GI no
funcionante pueden sobrevivir con nutrición parenteral total
durante años, pero se trata claramente de una medida provisio-
na
l 215 .El riesgo de complicaciones de la canulación de una vía
central aumenta con el tiempo, y los accesos vasculares en los niños
van quedando cada vez más limitados según se utilizan.
Hematología
Entre las urgencias hematológicas que pueden surgir en la UCI se
encuentran las alteraciones de la coagulación, de la inmunidad y
de la masa de eritrocitos. Estas anomalías pueden ser defectos
aislados primarios o ser secundarias a un fracaso multiorgánico
sistémico. El sistema inmunológico se analiza en la sección de
enfermedades infecciosas.
Sistema de la coagulación
La coagulación normal conlleva una fase inicial de formación de
un tapón hemostático de plaquetas y un segundo estadio de pro-
ducción de fibrina (vía intrínseca o extrínseca)
( fig. 74-2 ). Para que
tengan lugar las dos fases son esenciales las plaquetas, los factores
de la coagulación y un vaso sanguíneo intact
o 216,217 .Los neonatos
padecen una serie de trastornos de la coagulación medibles que
rara vez se asocian a manifestaciones clínicas. Los lactantes a
término y la mayoría de los prematuros muestran una interacción
normal entre plaquetas y vasos, pero la agregación plaquetaria se
encuentra alterada de forma transitoria. Además, muchos factores
de la coagulación se encuentran reducidos en concentración o acti-
vidad en el feto y en el recién nacido. Los factores más importantes
son los dependientes de la vitamina K: factores II, VII, IX y X. Éstos
se encuentran bajos al nacer y caen a unos niveles aún menores en
la primera semana de vida a menos que se administre vitamina K.
Los factores V y VIII se encuentran cercanos a los niveles del adulto
salvo en los lactantes más prematuros. Aunque las pruebas habitua-
les de estudio de la actividad de la coagulación se encuentran pro-
longadas en lactantes, la sangre de los recién nacidos se coagula más
rápido in vitro por la deficiencia de inhibidores naturales de la
proteasa, en especial de antitrombina II
I 216 .Diagnóstico de los trastornos hemostáticos
Los trastornos de la coagulación se diagnostican por la anamnesis,
la exploración física y los datos de laboratorio. Es necesario buscar
cualquier antecedente de hemorragia, hematomas, ingestión de fár-
macos, enfermedades asociadas o antecedentes familiares de hemo-
rragias. Hay que explorar al paciente meticulosamente para descartar
petequias o hematomas, hemorragias gingivales o hepatoesplenome-
galia. Hay que observar las zonas de hemorragia o venopunción en
busca de coágulos frescos o de goteo de sangre. Las pruebas de labo-
ratorio para la evaluación del TTP, del TP, del tiempo de trombina,
del recuento de plaquetas y de los tiempos de hemorragia aportan
información valiosa sobre la naturaleza del defecto hemostático.
Trastornos específicos de la coagulación
Trastornos congénitos
Se han descrito deficiencias hereditarias de la mayoría de los fac-
tores de coagulación, pero la hemofilia clásica (factor VIII) y la
enfermedad de Christmas (factor IX) suponen la mayoría de los
casos (v. cap. 25). Desde que se dispone de los tratamientos moder-
nos de reposición de los factores de coagulación, estos trastornos
sólo en raras ocasiones provocan hemorragias potencialmente
mortales que hacen preciso el ingreso en la UC
I 218 .D
eficiencia
de
factor
viii
o
hemofilia
A.
Se transmite
mediante herencia recesiva ligada al X y se da en 1 de cada 10.000
lactantes varone
s 219 .La gravedad de la enfermedad clínica viene
determinada por la cantidad de factor circulante: la afección es gra-
ve cuando se asocia con menos de un 1% de los niveles normales,
moderadamente grave cuando dichos niveles son del 1 al 5% y muy
leve con un porcentaje del 5 al 30% de los valores normales. Los
puntos más frecuentes de hemorragia son los espacios articulares,
pero ésta se puede producir también en la cavidad peritoneal, el
tracto GI, el músculo, la piel o el SNC. Los traumatismos graves o
la cirugía pueden provocar hemorragias extensas. Se llega al diag-
nóstico demostrando la presencia de un TTP elevado y de niveles
reducidos de factor VIII. El tratamiento requiere la administración
de factor VIII derivado del plasma o proteínas recombinantes.
E
nfermedad
de
von
W
illebrand
.
Esta enfermedad se
produce casi con tanta frecuencia como la hemofilia A y se trans-
mite a ambos sexos mediante herencia autosómica dominante. El
factor de von Willebrand (vWF) es una glucoproteína multimérica
producida por los megacariocitos y las células endoteliales. El vWF
se adhiere a la matriz subendotelial tras las lesiones vasculares.
Cambia su conformación y hace que las plaquetas se unan y activen.
La enfermedad de von Willebrand se clasifica en tres tipos. El tipo I
consiste en una reducción cuantitativa del vWF normal y supone
el 85% de los casos. En el tipo II el vWF es anómalo desde el punto
de vista cualitativo y en el tipo III no existe vWF. Los problemas
clínicos más frecuentes son las hemorragias de la piel y de las mem-
branas mucosas, especialmente epistaxis y menorragias. El TTP y
el tiempo de hemorragia se encuentran prolongados en este tras-
2448
Anestesia pediátrica
V
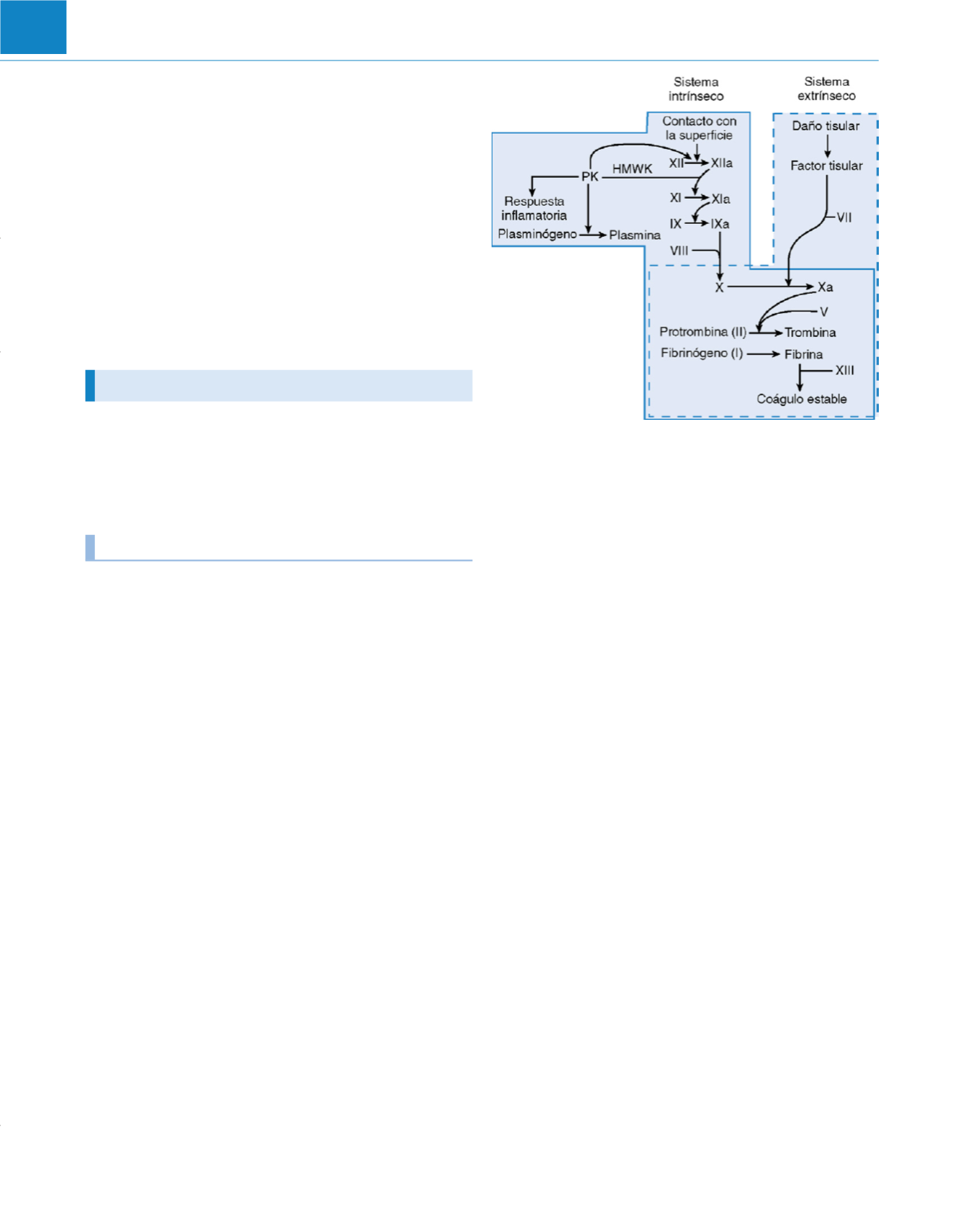
Figura 74-2
Esquema de la coagulación sanguínea. El sufijo «a» denota el factor
activado con la actividad enzimática. HMWK, cininógeno de alto peso molecular;
PK, precalicreína.
(Modificada de Hathaway WE: Hemostasis. En Rudolph AM [ed.]:
Pediatrics
, 17.
a
ed. East Norwalk, CT, Appleton-Century-Crofts, 1982, pág. 1110.)









