
disminuir la tasa de proteólisis periférica, lo que demuestra que la
aceleración de la producción hepática de glucosa no está relacio-
nada con el aumento del nivel de proteólisis periférica. El grado de
la pérdida de nitrógeno es proporcional al grado de estrés y dismi-
nuye a medida que el paciente se recupera. Después de sufrir que-
maduras graves, la proteólisis y la consecuente salida de aminoácidos
desde el músculo aumentan casi el doble. El aumento de la proteó-
lisis parece estar modulado sólo parcialmente por las hormonas de
estrés, específicamente el cortisol. Por el contrario, otros mediado-
res como el TNF-
a
, la IL-1 y la IL-6 y el interferón-
g
median en la
actividad catabólica. Precisamente, es el equilibrio entre esos media-
dores catabólicos y las hormonas anabolizantes como la insulina y
los factores de crecimiento insulinoides el que determina la magni-
tud del catabolismo. Hay varias rutas metabólicas responsables de
la proteólisis del músculo esquelético, como es la vía lisosomal de
proteólisis dependiente de ATP-ubiquitina y activada por Ca
2+
66 .El
hígado también contribuye al catabolismo al aumentar el aclara-
miento del
a
-amino nitrógeno (urea). Después de la cirugía, la tasa
de esta conversión aumenta al doble. El bloqueo de la secreción de
glucagón y cortisol con una combinación de etomidato, somatosta-
tina y anestesia epidural torácica disminuyó este aclaramiento, lo
que indicaría la participación del glucagón y, posiblemente, del
cortisol y de los reflejos nerviosos aferentes en este proceso.
Hay algunos datos contradictorios sobre la actividad de sín-
tesis de proteínas en el músculo esquelético durante el estrés.
Algunos estudios indican un descenso de la misma (p. ej., descenso
del 31% 24 horas después de la colecistectomía abierta) en el
músculo esquelético cuando se perfunde solución salina o NPT.
Las biopsias hepáticas obtenidas durante la cirugía demostraron el
descenso de la síntesis de proteínas hepáticas después de 20minutos
de cirugía, con un descenso aún mayor a medida que avanzaba la
cirugí
a 67. La síntesis de proteínas también disminuye en los tejidos
cuyas células se reproducen con rapidez, como los enterocitos, las
células del sistema inmunitario y los queratinocitos. Otros investi-
gadores también demuestran que el balance nitrogenado negativo
se debe a la aceleración de la proteólisis, que es mayor que el
aumento de la tasa de síntesis de proteínas. Además, las alteraciones
de metabolismo de las proteínas son importantes porque la admi-
nistración de NPT después de la colecistectomía abierta no previno
el descenso de la síntesis de proteínas musculares que se observa
24 horas después de la cirugía.
Los efectos nocivos del reposo prolongado en cama contri-
buyen aún más a las alteraciones del metabolismo de las proteínas
causadas por las hormonas de estrés y las citocinas después de
heridas y cirugía. En los voluntarios normales, 28 días de reposo
Nutrición y control metabólico
2701
85
Sección VII
Cuidados críticos
© ELSEVIER. Fotocopiar sin autorización es un delito
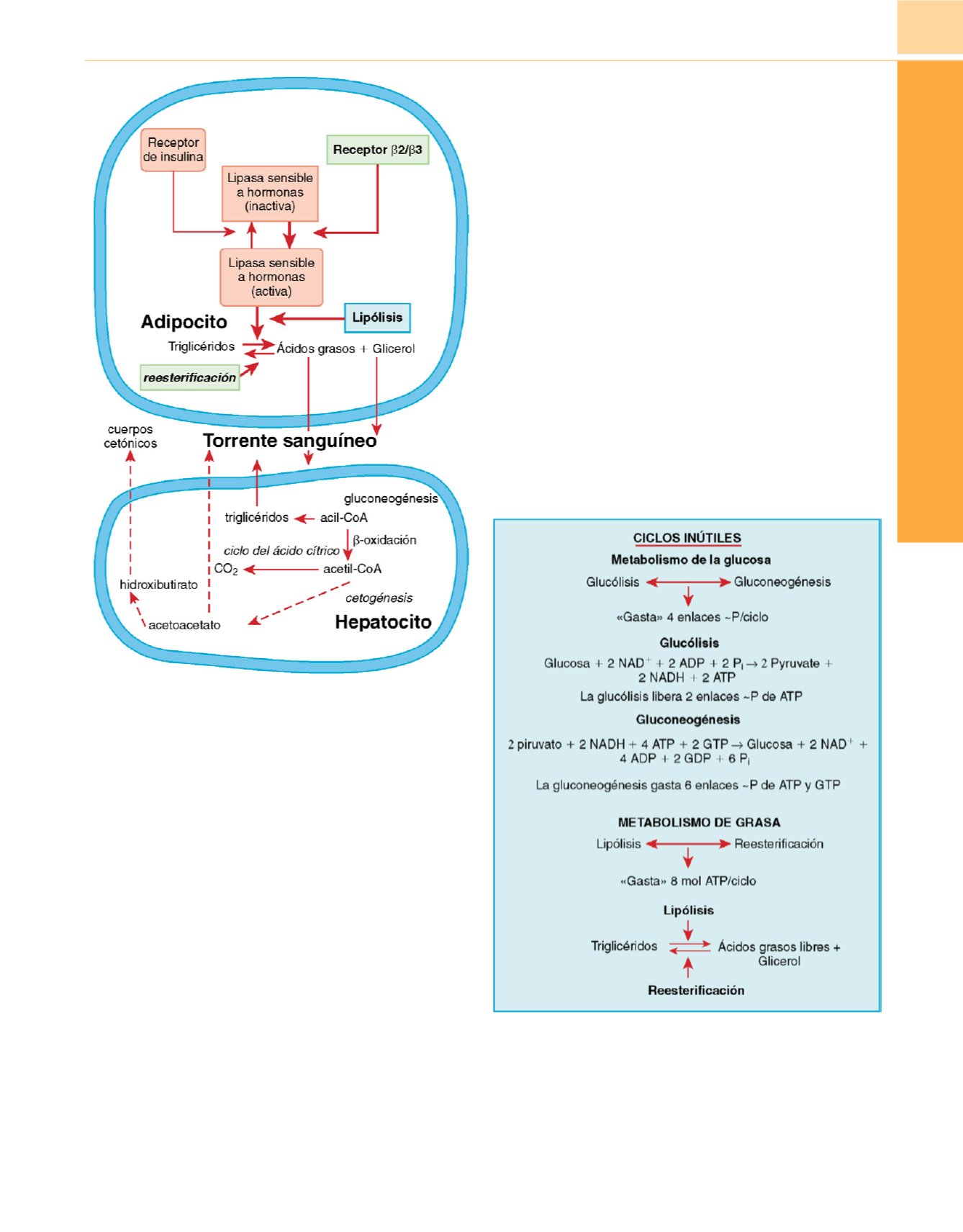
Figura 85-6
Metabolismo lipídico durante el estado de estrés. Las
catecolaminas estimulan los receptores
b
2
y
b
3
, activando la lipasa sensible a
hormonas y provocando lipólisis. Los ácidos grasos libres se transportan hacia
el hígado, donde sufren la
b
-oxidación y son la fuente principal de energía
durante el estrés (la palmitoil-CoA logra un rendimiento neto de 130 ATP).
El glicerol liberado a través de la lipólisis es el sustrato para la gluconeogénesis
y se convierte en glucosa. Como las concentraciones de insulina están
elevadas, la producción de cetonas no está aumentada. Tanto la lipólisis como
la reesterificación están aumentadas, con lo que el ciclo se vuelve inútil.
Figura 85-7
Dos ciclos inútiles que contribuyen al hipermetabolismo de la
respuesta al estrés. Uno de ellos consiste en un conjunto de reacciones
opuestas catalizadas por varias enzimas que actúan simultáneamente, al
menos con una de las reacciones dependiente de la hidrólisis del trifosfato
de adenosina (ATP), con lo que se produce calor. En el ciclo del metabolismo
lipídico se produce lipólisis neta, mientras que en el ciclo del metabolismo
de la glucosa se produce gluconeogénesis neta.
∼
P, enlace de fosfato de
alta energía, generalmente procedente del ATP.









