
Las velocidades de flujo de entrada altas (
≥
5 l/min) tienen
la ventaja de aumentar la previsibilidad de la concentración de
anestésico inspirado, pero con las desventajas de ser un derroche
y de aumentar la contaminación atmosférica. Las velocidades altas
de flujo de entrada pueden ser inaceptablemente caras por el
mayor consumo de anestésicos volátiles caros. También pueden
hacer que el gas inspirado sea más seco y aumentan la dificultad
para calcular la ventilación por los movimientos de la bolsa de
reinspiración. Estas desventajas van a favor del uso de técnicas
de flujo de entrada bajo.
Técnica de flujo bajo
o de circuito cerrado
Gran parte de la exposición previa presupone el uso de un sistema
sin reinspiración y una concentración fija de anestésico inspirado.
Aunque este método no anula los principios descritos con anterio-
ridad, tampoco refleja la diversidad de métodos aplicados en la
práctica. La práctica suele desviarse de dos formas: 1) la mayoría
de los anestesistas usan velocidad de flujo de entrada baja (flujo de
gas fresco) para ahorrar costes
( fig. 11-16 )y 2) la mayoría utilizan
una concentración alveolar constante y no una concentración ins-
pirada constante porque la concentración alveolar constante refleja
mejor un grado de anestesia constante.
Una baja velocidad de flujo de entrada tiene varias ventajas
y pocas desventajas, estas últimas relacionadas principalmente con
la cinética. Las ventajas de la administración de flujo de entrada
bajo (definida como un flujo de gas fresco inferior a la mitad del
volumen minuto, habitualmente
<
3 l/min) o anestesia de circuito
cerrado (definida como suministro de gases en cantidades suficien-
tes para sustituir sólo los gases, tanto anestésicos como oxígeno,
extraídos por el paciente) son: menor coste, aumento de la humi-
dificación, disminución de la pérdida de calor, disminución de la
liberación de anestésico al ambiente y mejor capacidad para evaluar
variables fisiológicas como la ventilación. Entre las desventajas,
aumenta la preocupación por la concentración de oxígeno (sobre
todo si se emplea óxido nitroso porque el paciente también aporta
nitrógeno de los depósitos corporales y este nitrógeno puede dis-
minuir ligeramente la concentración de oxígeno inspirado). Sin
embargo, la desventaja más preocupante es la ausencia de control
inherente a los flujos bajos y sobre todo a los circuitos cerrados.
Anestesia de circuito cerrado
El uso de un circuito cerrado representa un extremo de la admi-
nistración de anestesia, utilizado pocas veces porque pocos siste-
mas eliminan por completo la fuga de gas por el circuito. De hecho,
los anestesistas extraen aproximadamente 200ml/min para anali-
zar la concentración de oxígeno, dióxido de carbono y anestésico.
Habitualmente, la anestesia de circuito cerrado requiere la
sustitución de tres gases: 1) oxígeno, 2) óxido nitroso y 3) un anes-
tésico volátil potente. Cada sustitución implica ciertas considera-
ciones diferentes. La sustitución de oxígeno permanece constante
a menos que el metabolismo cambie como consecuencia de una
respuesta simpática a la estimulación, alteración de la temperatura
corporal o escalofríos. La sustitución de óxido nitroso sigue una
evolución bastante previsible, en parte porque la concentración
aplicada no varía habitualmente. Además, es uno de los anestésicos
menos solubles, sobre todo en grasa, y es el más propenso a la
pérdida percutánea (un valor constante). La captación de los anes-
tésicos inhalatorios potentes tiene más interés y posibilidad de
variación.
La captación de anestésicos potentes puede calcularse a
partir de los valores (constantes) obtenidos por Yasuda y cols
. 10,11en el ser humano. Estos valores pueden aplicarse para obtener la
captación a una concentración alveolar constante. Para conseguir
un grado adecuado de comparación he supuesto una concentra-
ción alveolar igual a la CAM. La
figura 11-17revela formas
paralelas para cada anestésico, formas determinadas por las carac-
terísticas de perfusión y disolución de los tres compartimentos
tisulares principales (más la difusión intertisular). Por tanto, una
captación inicial elevada disminuye rápidamente a una concentra-
ción mucho menor en 5 a 10 minutos como consecuencia de la
elevada captación inicial por el GRV (debido a su abundante per-
fusión) y del rápido descenso de la captación impuesto por una
constante de tiempo corta (la constante de tiempo se obtiene de la
relación entre la capacidad de un sistema y el flujo a través del
sistema, y resulta útil porque indica el tiempo necesario para que
ocurra un cambio del 63% en el sistema). El consiguiente descenso
menos pronunciado se debe principalmente a la mayor constante
de tiempo del GM que domina este período hasta que su captación
disminuye por debajo de la proporcionada por el cuarto compar-
timento y el GG.
Aunque las curvas de cada anestésico no difieren en la forma,
tienen posiciones diferentes. La altura de cada curva (es decir, la
captación) es directamente proporcional a dos factores: solubilidad
y CAM. Esta relación tiende a reducir las diferencias entre los
anestésicos porque la solubilidad y la CAM tienden a moverse de
forma inversa. Por ejemplo, aunque la CAM del desflurano es cinco
veces la del isoflurano, la captación del desflurano es menos del
doble que la del isoflurano por la menor solubilidad del desflurano
tanto en sangre como en tejidos.
Es posible calcular la captación a partir de la «regla de
la raíz cuadrada del tiempo», propuesta por primera vez por
Anestésicos inhalatorios: captación y distribución
317
11
Sección II
Farmacología y anestesia
© ELSEVIER. Fotocopiar sin autorización es un delito
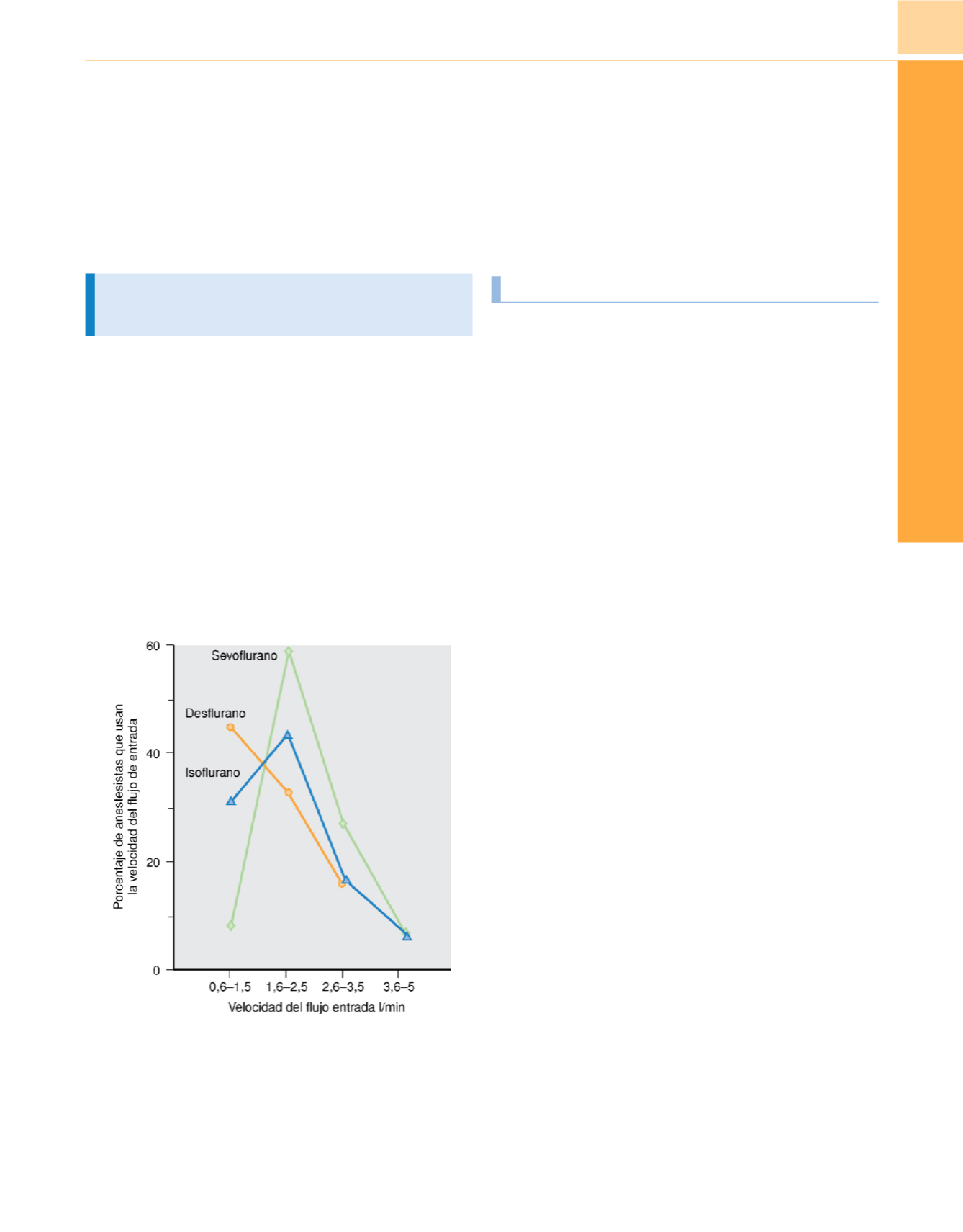
Figura 11-16
En 2005 se hizo una encuesta a los anestesistas sobre las
velocidades del flujo de entrada que usaban habitualmente para mantener la
anestesia. Las respuestas eran muy diversas aunque la mayoría utilizaba
sistemas de flujo bajo con una velocidad de flujo de entrada
≤
2 l/min.
(Datos
no publicados del
Inform Research Flow Rate Tracking Study,
mayo de 2005,
aportado como comunicación personal por Baxter Healthcare Corp. A E.I
Eger II.)









