
y en la médula espina
l 479. Debe señalarse que la calidad de la sedación
que produce la dexmedetomidina parece ser distinta a la que provo-
can otros fármacos sedantes que actúan sobre los sistemas GABA. Se
ha descrito que los pacientes a los que se les administra una infusión
de dexmedetomidina como parte de su régimen de sedación en el
postoperatorio en la UCI son fácilmente despertables y capaces de
responder a órdenes y cooperar, aunque permanezcan con intubación
endotraqueal. Cuando no se les molesta, los pacientes vuelven a dor-
mirse inmediatament
e 480. A pesar de que con la dexmedetomidina se
consiguen niveles de sedación profundos, la depresión respiratoria es
limitada, lo que proporciona amplios márgenes de segurida
d 481 .Esta
característica permite realizar test de «despertar diario» de forma
segura. Estas pruebas críticas, que consisten en retirar a los pacientes
de la UCI en ventilación asistida todos los fármacos sedantes para
valorar su estado mental y ajustar la sedación, acorta la duración de
la ventilación y de la estancia en la UC
I 482 .Los agonistas
a
2
ejercen sus efectos sedantes actuando sobre
las vías que promueven el sueño de forma endógena (v.
fig. 16-21).
La dexmetomidina produce una disminución de la actividad de las
proyecciones del locus ceruleus al núcleo preóptico ventrolateral. Esta
acción aumenta la liberación GABAérgica y de galanina en el núcleo
tuberomamilar y, como consecuencia, reduce la liberación de hista-
mina en las proyecciones corticales y subcorticale
s 483 .Los agonistas
a
2
parecen inhibir el paso de iones por los canales de calcio de tipo
L y P, y facilitan el paso a través de los canales de calcio dependientes
de voltaje activados por potasi
o 484. Se especula con que la similaridad
entre el sueño natural (sin movimientos rápidos de ojos, no-REM) y
la hipnosis inducida por la dexmedetomidina mantiene la función
cognitiva e inmunológica en los estados de privación de sueño (como
en la UCI
) 485. La dexmetomidina puede producir una profunda seda-
ción, y se ha utilizado como anestesia i.v. total con dosis 10 veces
superiores a las del rango normal para la sedació
n 486 .Los agonistas
a
2
tienen la ventaja de que sus efectos se pueden
revertir fácilmente por los antagonistas
a
2
adrenérgicos (p. ej., el
atipamezol
) 487. El atipamezol no está aprobado al día de hoy para su
uso en seres humanos. Al igual que otros receptores adrenérgicos,
los agonistas
a
2
producen tolerancia después de su administración
durante períodos prolongado
s 488. Como la dexmedetomidina sólo se
ha aprobado por la FDA para sedaciones de corta duración (de hasta
24 horas), la tolerancia, la dependencia o la adicción no constituyen
un problema. Por el contrario, la dexmedetomidina se puede utilizar
para tratamiento de adicciones; se ha utilizado para la desintoxica-
ción rápida de los opioides, la privación de cocaína y la tolerancia
iatrogénica, tras sedación prolongada, con benzodiazepinas u opioi-
de
s 489.En animales,la dexmedetomidina,al contrario que los opioides,
no produce hiperalgesia ni alodinia después de su suspensió
n 490 .Las
ratas que presentaban tolerancia a la morfina también mostraron
una menor eficacia a los efectos hipnóticos y analgésicos de la dex-
medetomidina. A medida que se mejoraba la tolerancia a los opioi-
des, se recuperaba antes el efecto hipnótico de la dexmedetomidina,
con lo que se recuperaba su efecto analgésic
o 491 .Estos datos indican
que posiblemente exista una tolerancia cruzada entre receptores.
Analgesia
Los efectos analgésicos de la dexmedetomidina son complejos. Los
agonistas
a
2
tienen un efecto analgésico cuando se inyectan por vía
intratecal o epidura
l 492. La administración de clonidina en el neuroeje
es útil en el dolor agudo, dolor oncológico y dolor neuropátic
o 493,494.
Anestésicos intravenosos
519
16
Sección II
Farmacología y anestesia
© ELSEVIER. Fotocopiar sin autorización es un delito
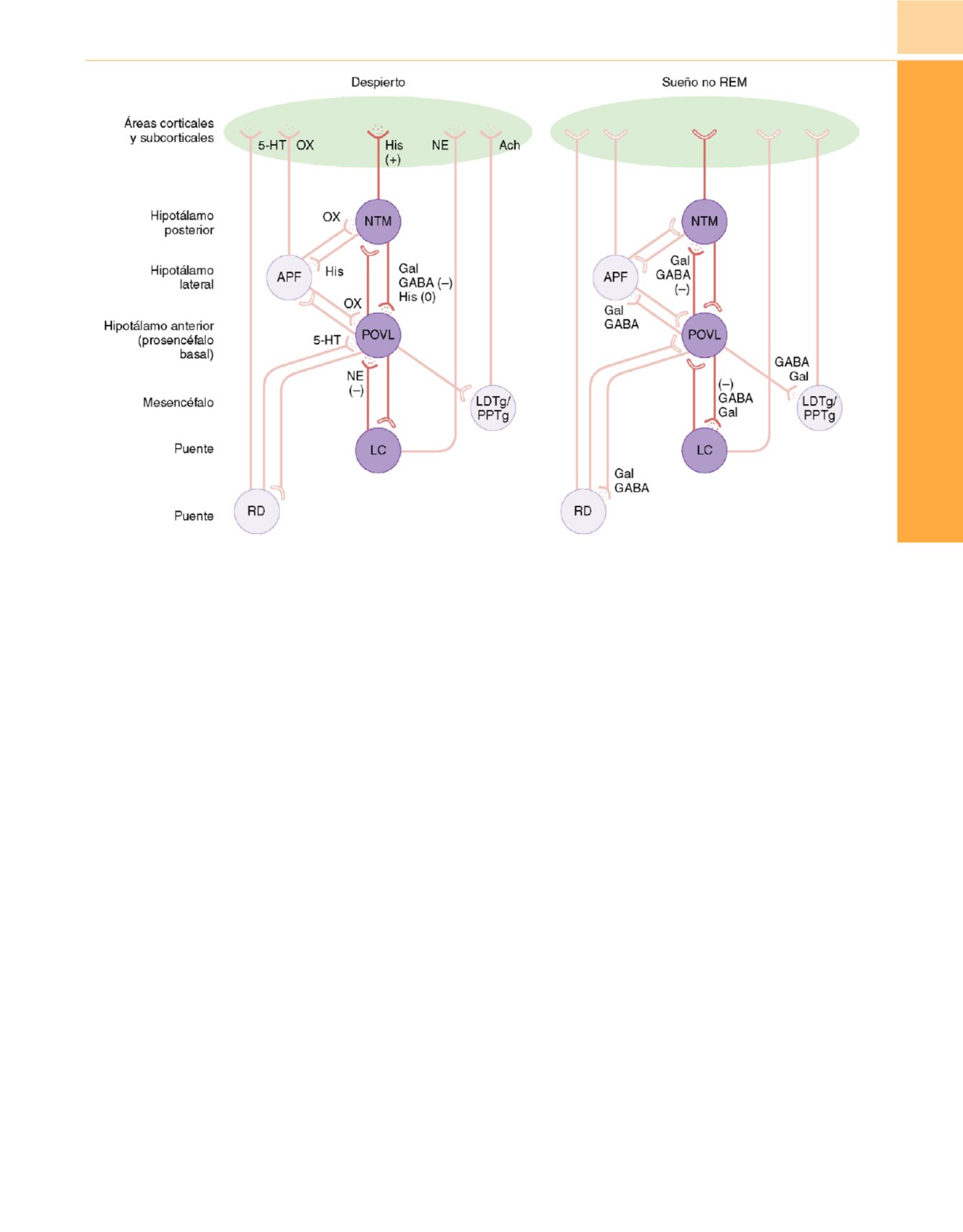
Figura 16-21
Se ha demostrado que la dexmedetomidina induce un patrón de sueño no REM. La estimulación del locus caereuleus (LC) por la
dexmedetomidina
(diagrama derecho)
libera la inhibición que el LC produce sobre el núcleo preóptico ventrolateral (POVL). A continuación, el POVL libera
ácido
g
-aminobutírico (GABA) sobre el núcleo tuberomamilar (NTM). Esto inhibe la liberación de la histamina, promotora del estado de alerta/despertar sobre la
corteza y el prosencéfalo, induciendo así la pérdida de consciencia. APF, area perifornical; RD, rafe dorsal.
(De Ebert T, Maze M: Dexmedetomidine: Another
arrow for the clinician’s quiver.
Anesthesiology
101:569-570, 2004.)









