
volumen de distribución, como la enfermedad hepática o renal, las
concentraciones plasmáticas precoces del fármaco pueden ser infe-
riores a las que se observan cuando la función del órgano es normal;
cuando el volumen de distribución es mayor, la concentración
plasmática debería ser menor, mientras que la cantidad total de
fármaco debería ser más elevada (
fig. 19-16 ). Una reducción de la
unión a proteínas del fármaco causa un incremento del volumen
de distribución, pero como el grado de unión a proteínas de los
bloqueantes neuromusculares es pequeño, los cambios en la unión
a proteínas tendrán un efecto mínimo sobre su distribució
n 128 .La recuperación de la función neuromuscular se produce
cuando las concentraciones plasmáticas disminuyen, y la mayor
parte de esta reducción se produce debido a la distribución. Por
tanto, los procesos que afectan sobre todo a la eliminación del
fármaco, como la insuficiencia renal, pueden no estar asociados a
una duración prolongada del bloque
o 129,130 .Sin embargo, conforme
la recuperación pasa a depender más de la eliminación del fármaco
que de su distribución (es decir, del 25 al 75% o más) o después de
la administración de dosis más altas o repetidas, la duración de la
acción se puede prolonga
r 123,131 .Tras la inyección de un bloqueante neuromuscular, la con-
centración plasmática del fármaco empieza a disminuir de forma
inmediata. El efecto (bloqueo neuromuscular) comienza en 1 mi
nuto, aumenta al principio y no se recupera hasta pasados muchos
minutos a pesar de que la concentración plasmática del fármaco
disminuye de forma continua. Esta discrepancia entre la concen-
tración plasmática y el efecto del fármaco se produce porque la
acción de los bloqueantes neuromusculares no tiene lugar en el
plasma, sino en la unión neuromuscular. Para producir parálisis, el
fármaco debe difundir desde el plasma a la unión neuromuscular
y el efecto termina luego gracias a la difusión del fármaco nueva-
mente hacia el plasma (v.
fig. 19-15 ). Por tanto, las concentraciones
en la unión neuromuscular muestran un desfase respecto a las
concentraciones plasmáticas, y son menores cuando se inicia el
bloqueo y mayores durante la recuperación. La relación concentra-
ción plasmática-efecto muestra histéresis, es decir, para un nivel de
bloqueo determinado las concentraciones plasmáticas son más
altas durante el inicio que durante la recuperación. Por esta razón,
no es posible obtener una relación concentración-efecto relacio-
nando simplemente la concentración plasmática con el nivel de
bloqueo neuromuscular.
Para superar este problema se han desarrollado modelos
farmacodinámicos que incorporan un factor que se corresponde
con el retraso causado por la difusión del fármaco hacia y desde la
unión neuromuscula
r 84,120,132-143. Este factor, k
e0
, es la constante de
velocidad para el equilibrado del fármaco entre el plasma y la unión
neuromuscular. Al medir las concentraciones plasmáticas del
fármaco y el bloqueo neuromuscular durante las fases de inicio y
recuperación, y utilizando la técnica de modelado farmacocinético
y farmacodinámico simultáneo, se puede evitar la histéresis de la
curva de concentración plasmática-efecto, hacer una estimación de
las concentraciones reales del fármaco en la unión neuromuscular
y derivar las relaciones concentración-efecto reales (Ce
50
y k
e0
) para
los bloqueantes neuromusculares
( tabla 19-5 ) 120.
Manejo clínico
Los bloqueantes neuromusculares se usan principalmente para
facilitar la intubación traqueal y conseguir la relajación quirúrgica.
La intensidad del bloqueo neuromuscular necesaria depende del
tipo de procedimiento quirúrgico. Surgen aspectos de seguridad
importantes cuando se utilizan bloqueantes neuromusculares:
efectos secundarios respiratorios y cardiovasculares y la adecua-
ción de la recuperación de la función neuromuscular normal.
Existen varias alternativas para los bloqueantes neuromus-
culares que consiguen una relajación quirúrgica adecuada. Es
importante recordarlas todas para evitar confiar exclusivamente en
el bloqueo neuromuscular para alcanzar el grado de relajación
deseado. Entre estas opciones se encuentran el ajuste de la profun-
didad de la anestesia general, el uso de la anestesia regional, una
buena colocación del paciente en la mesa de quirófano y el ajuste
adecuado de la profundidad del bloqueo neuromuscular. La selec-
ción de una o varias de estas opciones viene determinada por el
tiempo estimado que queda de intervención, por la técnica anesté-
sica y por la maniobra quirúrgica necesaria.
Dosis
Recomendaciones generales sobre dosis
Es importante elegir la dosis adecuada de un bloqueante neuro-
muscular no despolarizante para garantizar que se obtiene el efecto
deseado sin sobredosis
( tablas 19-6 y 19-7). Además de los cono-
cimientos generales sobre estas recomendaciones, la práctica
correcta pasa por utilizar un estimulador de nervio periférico para
ajustar la dosis de relajante al paciente concreto. Se deben evitar las
sobredosis por dos motivos: limitar la duración del efecto del
fármaco para adaptarla a la duración estimada de la cirugía y evitar
efectos secundarios de tipo cardiovascular no deseados.
Dosis inicial y de mantenimiento
La dosis inicial viene determinada por el fin de la administración.
Tradicionalmente, las dosis empleadas para facilitar la intubación
traqueal son dos veces la DE
95
(estas dosis se aproximan a cuatro
veces la DE
50
) (v.
tabla 19-6). Si la tráquea ya se ha intubado sin
usar un bloqueante no despolarizante o con succinilcolina y el
objetivo es sólo conseguir la relajación quirúrgica, hay que admi-
nistrar una dosis ligeramente inferior a la DE
95
(v.
tabla 19-7),
ajustándola al alza en función de las respuestas evocadas por la
estimulación del nervio periférico. Los ajustes a la baja de la dosis
inicial son necesarios en presencia de cualquiera de los anestésicos
inhalados potentes (v. la subsección sobre interacciones medica-
mentosas más adelante).
Para evitar que se produzca una parálisis prolongada resi-
dual o un antagonismo inadecuado del bloqueo residual, o ambos,
640
Farmacología y anestesia
II
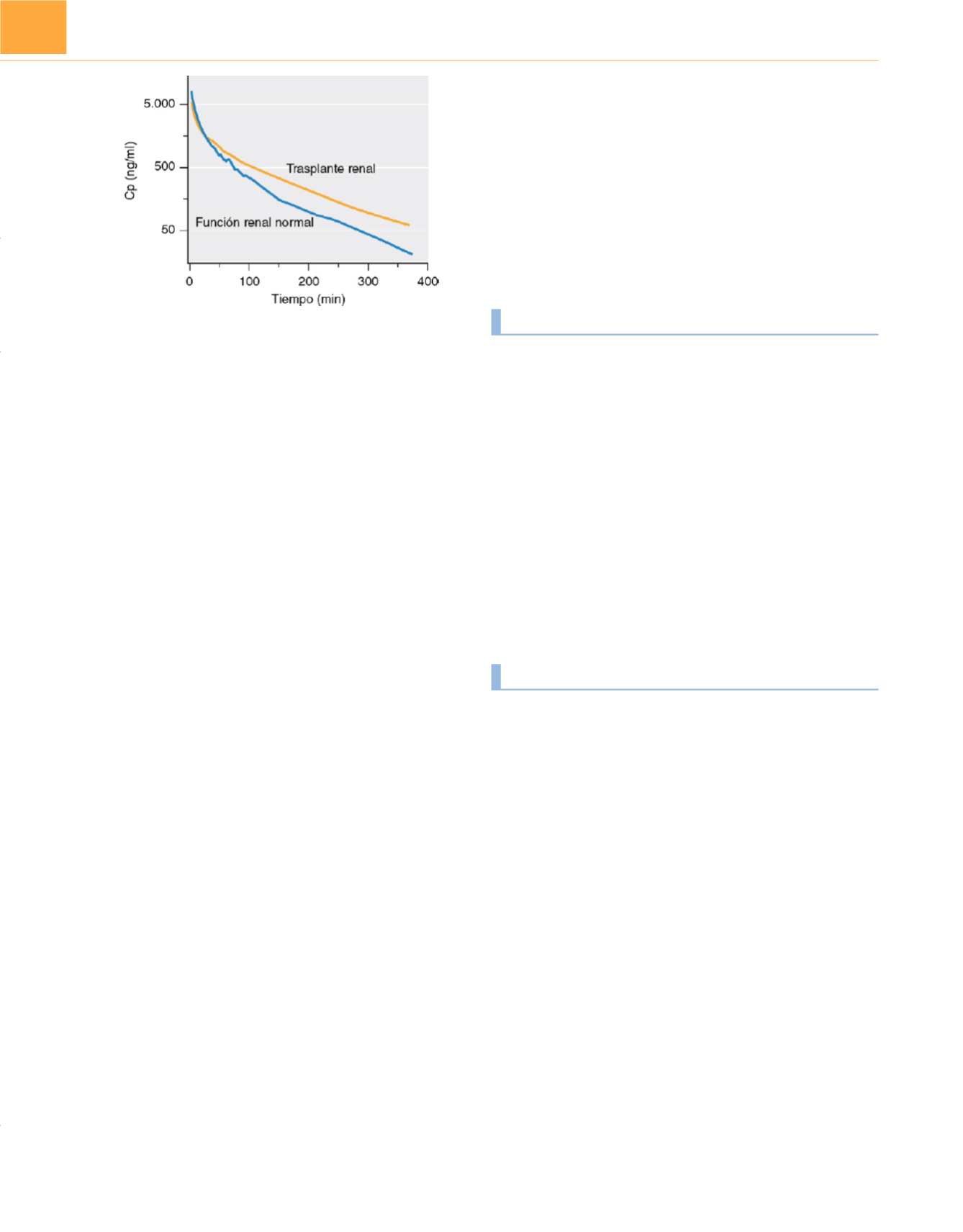
Figura 19-16
Concentración plasmática (Cp) «promedio» frente al tiempo
después de administrar una dosis de 0,6mg/kg de rocuronio a pacientes con
una función renal normal
(línea azul)
o a pacientes sometidos a un trasplante
renal
(línea amarilla). (De Szenohradszky J, Fisher DM, Segredo V y cols.:
Pharmacokinetics of rocuronium bromide (ORG 9426) in patients with normal
renal function or patients undergoing cadaver renal transplantation.
Anesthesiology
77:899-904, 1992.)









