
nos han ofrecido una variante conocida como «hiato aniónico
corregido»:
Hiato aniónico corregido (por la albúmina) =hiato aniónico calcu-
lado+2,5× (albúmina normal [en g/dl] −albúmina observada [en
g/dl])
El segundo punto débil de este abordaje es el uso del bicar-
bonato en la ecuación. Se puede producir una alteración de la
concentración de [HCO
3
−
] por motivos independientes de un tras-
torno metabólico (p. ej., hiperventilación). El déficit de bases y el
hiato aniónico con frecuencia infraestiman la magnitud del tras-
torno metabólic
o 18 .Sin embargo, el hiato aniónico es útil para
diferenciar la acidosis por aniones no medidos de la acidosis hiper-
clorémica en un paciente previamente sano (p. ej., en un trauma-
tismo agudo).
Abordaje de Stewart-Fencl
Se puede obtener un reflejo más exacto del estado acidobásico
verdadero utilizando el abordaje de Stewart-Fenc
l 1,2. Este abordaje
se basa en el concepto de neutralidad eléctrica, una pequeña mejora
respecto al hiato aniónico. En el plasma hay una DIF [(Na
+
+Mg
2+
+Ca
2+
=K
+
) − (Cl
−
+A
−
] 40-44mEq/l, equilibrada por la carga nega-
tiva del bicarbonato y A
TOT
(la base amortiguadora). Hay una
pequeña diferencia entre la DIF aparente (DIF apa-
rente= ([Na
+
] + [K
+
] + [Mg
2+
] + [Ca
2+
]) − [Cl
−
]) y la base amortigua-
dora. Esta DIF efectiva= [HCO
3
−
] + [carga de la albúmina] + [carga
del Pi] (en mmol/l). Como los ácidos débiles como la albúmina y
el fosfato tienen grados conocidos de ionización, se puede calcular
el HAG, que cuantifica la cantidad de aniones no medidos presen-
tes
( fig. 39-5):
[alb
−
]=[alb] (en g/l)×(0,123×pH−0,631)
[Pi] (en mg/dl)=[Pi]/10×pH−0,47
HIF=DIF aparente−DIF efectiva
La DIF cambia cuantitativamente en términos absolutos y
relativos cuando hay cambios de la concentración plasmática de
agua. Fencl y cols
. 18abordaron este fenómeno corrigiendo la con-
centración de cloruro por el agua libre (Cl
−
corr
) utilizando la
ecuación siguiente:
[Cl
−
]
corregida
= [Cl
−
] observada× ([Na
+
] normal/[Na
+
]
observada)
Esta concentración de cloruro corregida se puede insertar en la
ecuación de la DIF aparente. De igual forma, el valor derivado de
los aniones no medidos se debe corregir por el agua libre utilizan
do los aniones no medidos en lugar del Cl
−
en la ecuación ante
rior
18
. En una serie de nueve personas normales, Fencl y cols
. 18esti
maron el valor «normal» de HAF como 8 ± 2mEq/l.
Aunque es exacto, el HAG es difícil y costoso, siendo nece-
saria la medición de múltiples iones y de la albúmina. Un abordaje
alternativo, utilizado por Gilfix y cols
. 49y posteriormente por Bala-
subramanyan y cols.
45y Story y cols.
, 50es calcular el hiato del
déficit-exceso de bases. Esto permite recalcular el DEB utilizando
los iones fuertes, el agua libre y la albúmina. El hiato de déficit y el
exceso de bases resultante deben reflejar el HAG y el hiato aniónico.
Encontramos que el cálculo simplificado de Story y cols
. 50tiene la
máxima utilidad
( tabla 39-1 ). Estos investigadores utilizan dos
ecuaciones para calcular el DEB para el sodio, el cloruro y el agua
libre (DEB
NaCl
) y para la albúmina.
Es probable que ningún número único permita que los
investigadores expliquen por completo los trastornos acidobásicos
complejos. Fencl y cols
. 18señalaron que en lugar de centrarse en el
hiato aniónico o el DEB, los médicos deben abordar cada uno de
los gases sanguíneos en relación con todos los efectos alcalinizantes
o acidificantes: acidosis o alcalosis respiratoria, presencia o ausen-
cia de DIF anormal (debido a exceso o déficit de agua, electrólitos
medidos o electrólitos no medidos) y A
TOT
anormal.
Equilibrio acidobásico perioperatorio
1331
39
Sección III
Control de la anestesia
© ELSEVIER. Fotocopiar sin autorización es un delito
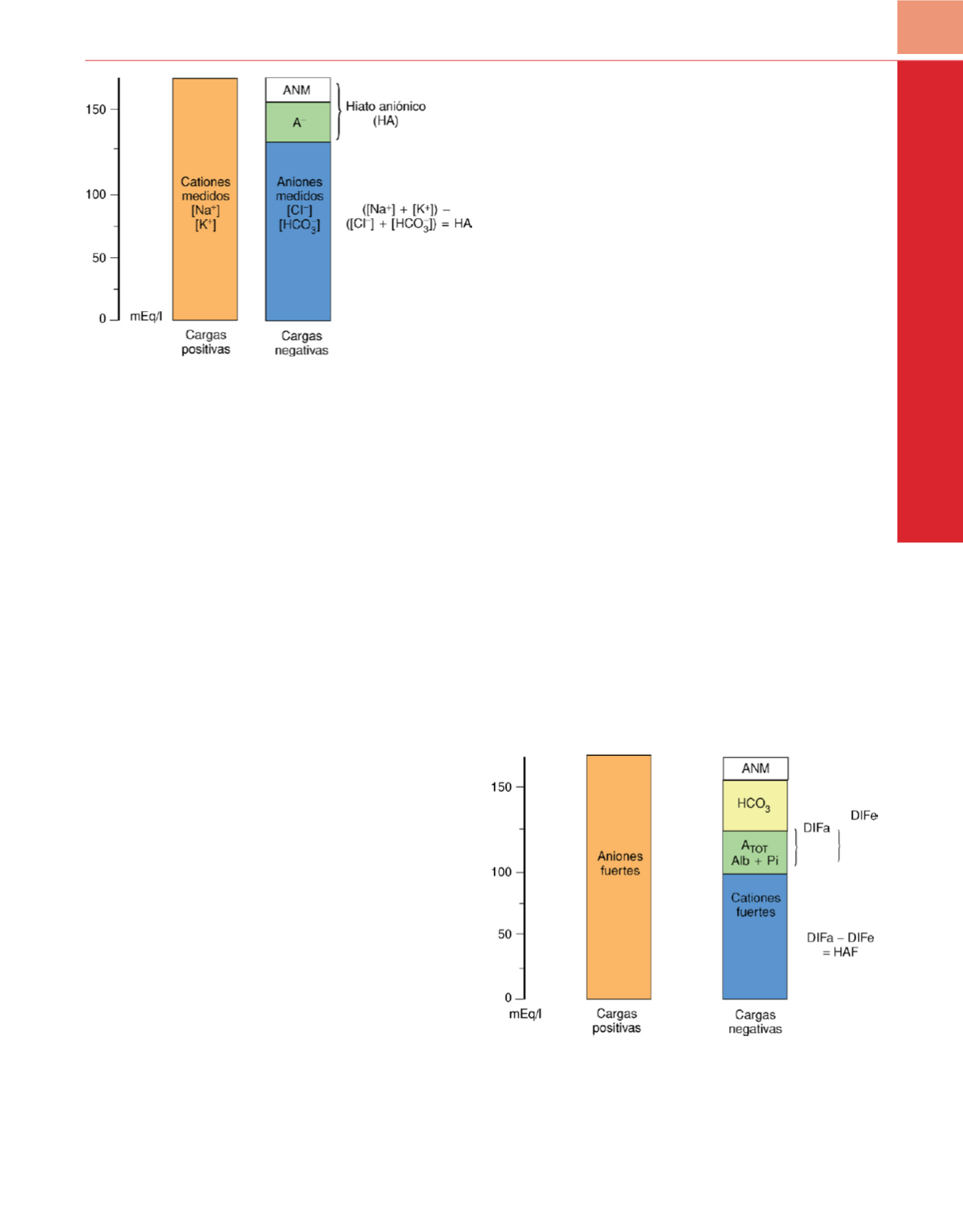
Figura 39-4
El hiato aniónico representa la diferencia de carga entre los
cationes medidos y los aniones medidos. La carga negativa que falta está
formada por ácidos débiles (A
−
), como albúmina y fosfato, y aniones no
medidos (ANM) fuertes, como lactato. El abordaje del hiato de aniones
fuertes (HAF) probablemente sea el método más exacto para evaluar los
trastornos acidobásicos y predecir la evolución
42-45
. La desventaja de este
sistema es que el HAF no representa los aniones fuertes no medidos, sino
todos los aniones que no se han medido. No está claro si esta desventaja es
clínicamente significativa, porque cada vez hay más datos de que la «acidosis
de estrés» se asocia a una mezcla de subproductos metabólicos, con
frecuencia sin elevación del lactato sérico. La presencia de un HAF
ensanchado se asocia a peor evolució
n 46,47 .Esto es importante, porque
muchos médicos de cuidados críticos siguen subestimando la importancia
del lactato en la evaluación y la determinación del pronóstico de las lesiones
grave
s 48 .Figura 39-5
El hiato de iones fuertes. La diferencia de iones fuertes aparente
(DIFa) es la suma de la concentración total de ácidos débiles (A
TOT
) más la
concentración del ion bicarbonato ([HCO
3
−
]). La diferencia de iones fuertes
efectiva (DIFe) es la DIF real. La diferencia entre ambas está formada por los
aniones no medidos (ANM).









