
Anestesia para la cirugía robótica
2161
66
Sección IV
Anestesia por subespecialidades en el adulto
© ELSEVIER. Fotocopiar sin autorización es un delito
capaz de desconectar con rapidez el dispositivo robótico si se
produce una urgencia de la vía respiratoria o de la anestesia. Al
igual que sucede en cualquier procedimiento laparoscópico que
requiera un neumoperitoneo presurizado con CO
2
, puede que se
precisen ajustes del ventilador para normalizar el CO
2 20espirado.
Algunos cirujanos alegan que el beneficio de la monitorización
arterial invasiva no supera los riesgo
s 19 .Este aspecto debería con-
siderarse en cada paciente en función de un análisis de riesgo/
beneficio.
Cirugía cardíaca
La aplicación de los instrumentos endoscópicos convencionales ha
preparado el camino para que varios procedimientos cardíacos se
realicen con ayuda robótica
(v. cap. 50 ). Nata
f 21realizó en 1997 la
técnica de obtención de arteria torácica interna con éxito. En 1998,
Loulmet y cols
. 22publicaron la primera cirugía de derivación arte-
rial coronaria completamente endoscópica. Las aplicaciones cardio-
torácicas de la cirugía asistida por robot han aumentado e incluyen
el cierre de la comunicación interauricula
r 23-25 ,la valvuloplastia
mitra
l 26 ,la ligadura del conducto arterioso permeabl
e 27, el injerto
de derivación arterial coronaria completamente endoscópic
o 28,29,
la cirugía mínimamente invasiva de la fibrilación auricula
r 30,31y la
colocación de electrodos de marcapasos de ventrículo izquierd
o 32.
Incluso aunque los avances técnicos en cirugía mínimamente
invasiva hayan introducido técnicas que se realizan mediante inci-
siones diminutas y al final pueden dejar obsoleta la esternotomía
quirúrgica, los cirujanos aún deben formarse y prepararse para con-
vertir la técnica en una esternotomía abierta si surge la necesidad.
La esternotomía por sí sola conlleva un riesgo limitado de morbili-
dad debido a la respuesta inflamatoria, aunque es ciertamentemenor
que el de la exposición a circulación extracorpóre
a 33-35 .Es obligatorio contar con conocimientos y experiencia en
anestesia cardíaca y torácica, pues ambos sistemas orgánicos deben
controlarse de forma segura. Hay que ser capaz de realizar y man-
tener una ventilación monopulmonar, así como el control de sus
consecuencias fisiológicas
( tabla 66-1). Está indicada la valoración
preoperatoria de la función pulmonar si el paciente presenta una
neumopatía significativa. Un mal resultado de estas pruebas puede
ser una contraindicación para la cirugía cardíaca asistida por robot,
porque la ventilación monopulmonar puede tolerarse mal. La
cirugía robótica puede requerir una prolongada ventilación mono-
pulmonar sin precedentes, que desafía los límites de nuestro cono-
cimiento sobre la fisiología respiratoria. Lamonitorización continua
de la función cardíaca mediante ecografía transesofágica (ETE) se
ha convertido en un estándar de asistencia sistemático y ha abierto
el camino a varios procedimientos requeridos para una cirugía
asistida por robot más segura.
Cirugía valvular mitral e implicaciones anestésicas
En 1997, dos grupos independientes publicaron la primera valvu-
loplastia mitral asistida por robo
t 36,37. En noviembre de 2002 la
FDA aprobó el uso de esta cirugía para realizar las valvuloplastias
mitrales. Estas intervenciones, realizadas al principio a través de
incisiones de minitoracotomía, podrían realizarse por completo a
tórax cerrado. Sin embargo, la sustitución valvular mitral puede
requerir aún una pequeña toracotomía para introducir la nueva
válvula protésica.
La cirugía valvular mitral que emplea aparatos robóticos se
realiza en unos pocos centros cardíacos de Estados Unidos y Europa.
Las técnicas anestésicas y otras consideraciones relevantes se han
descrito con anteriorida
d 38 .Los pacientes se evalúan al inicio
mediante cateterismo cardíaco para estimar el grado de estenosis
arterial coronaria y para valorar la función valvular. La regurgitación
mitral grave es un problema mecánico que requiere tratamiento
quirúrgico. La mayoría de los pacientes reciben tratamiento médico
con fármacos que reducen la poscarga, como los inhibidores de la
enzima convertidora de angiotensina (IECA) si son hipertensos.
Una aurícula izquierda hipertrófica suele ser susceptible de fibrila-
ción auricular y los pacientes que la presentan de forma persistente
pueden estar tomando anticoagulantes asociados al tratamiento del
control de la frecuencia. La elevación crónica de la presión auricular
izquierda puedemanifestarse con hipertensión pulmonar, que puede
agravarse aún más por una neumopatía obstructiva. La hipertensión
pulmonar grave contraindica la cirugía robótic
a 39 .Se coloca una vía intravenosa periférica de gran calibre. Se
proporciona sedación superficial con midazolam y anestesia local
antes de insertar vías arteriales radiales bilaterales. El paciente se
monitoriza del modo habitual con las derivaciones II y V
5
de ECG,
pulsioximetría y una vía de presión arterial derecha radial para
excluir la mala colocación del balón endovascular aórtico. Los
modernos monitores de ECG pueden proporcionar un análisis
automático del segmento ST para detectar la isquemia. Tras una
oxigenación abundante, el paciente se anestesia con una combina-
ción de midazolam, fentanilo e isoflurano, además de administrarle
un relajante muscular.
La tráquea se intuba mediante un tubo endotraqueal de
doble luz. La adecuada colocación del tubo se confirma mediante
broncoscopia. Se inserta una sonda de ETE para valorar la función
cardíaca y valvular, así como para guiar la colocación de una vía
central. Se utiliza una proyección medioesofágica, bicava a 90 grados para guiar la colocación de las cánulas de vena cava superior
(VCS) y de vena cava inferior (VCI)
( fig. 66-10 ). Al principio se
inserta un catéter introductor izquierdo del calibre 9 de French
mediante la técnica de Seldinger y se hace flotar un catéter de
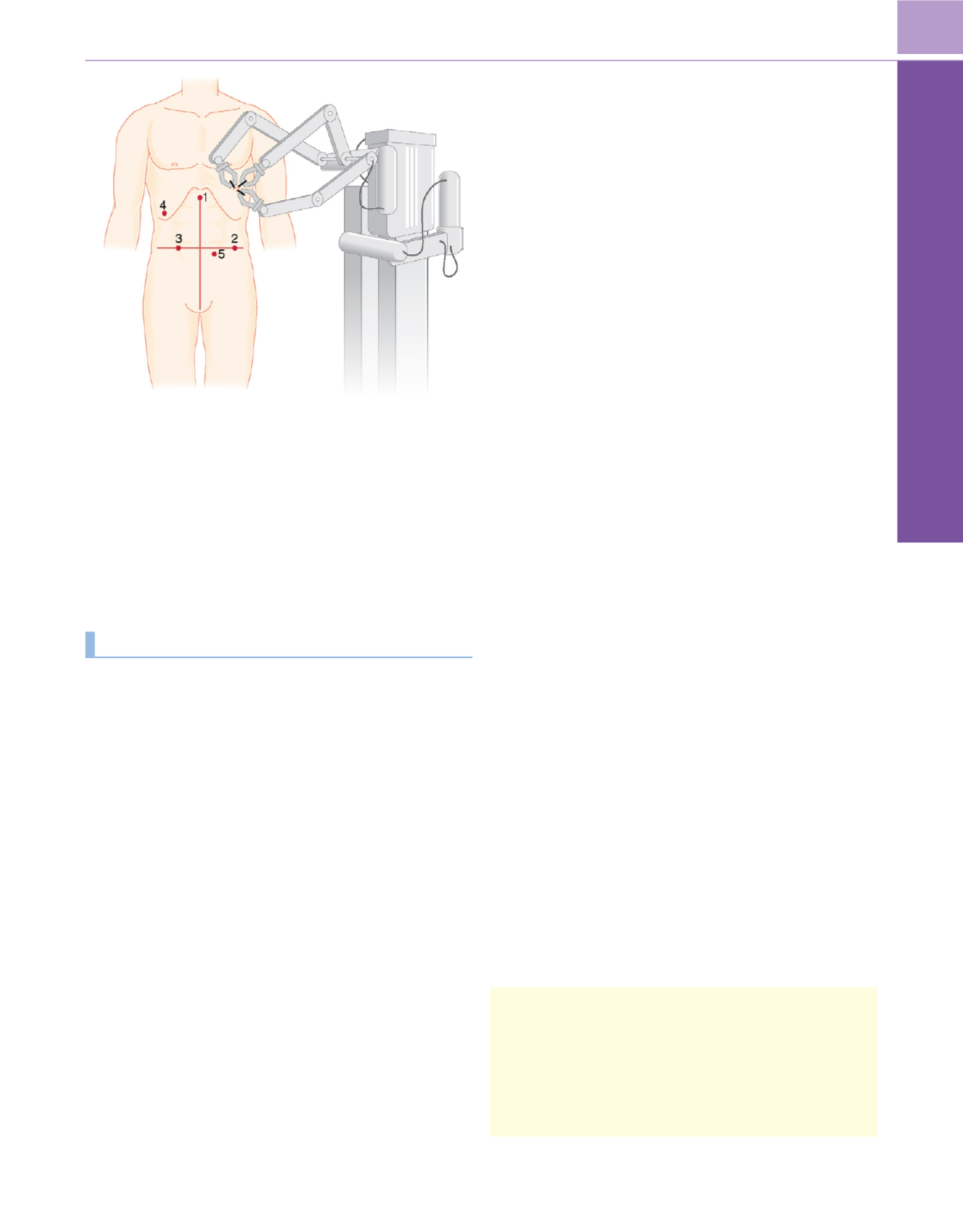
Figura 66-9
Puntos de incisión numerados para la colecistectomía y
localización de los brazos robóticos.
Tabla 66-1
Estrategia de ventilación monopulmonar
1. Emplear una F
io
2
=1
2. Comenzar la ventilación monopulmonar con ventilación de presión
controlada y mantener una presión meseta inferior a 30 cmH
2
O
3. Ajustar la frecuencia respiratoria de modo que la Pa
co
2
se aproxime a
40 mmHg
4. Comprobar la gasometría arterial
5. Aplicar presión positiva continua en la vía respiratoria en el pulmón no
ventilado
6. Aplicar presión positiva teleespiratoria en el pulmón ventilado









