
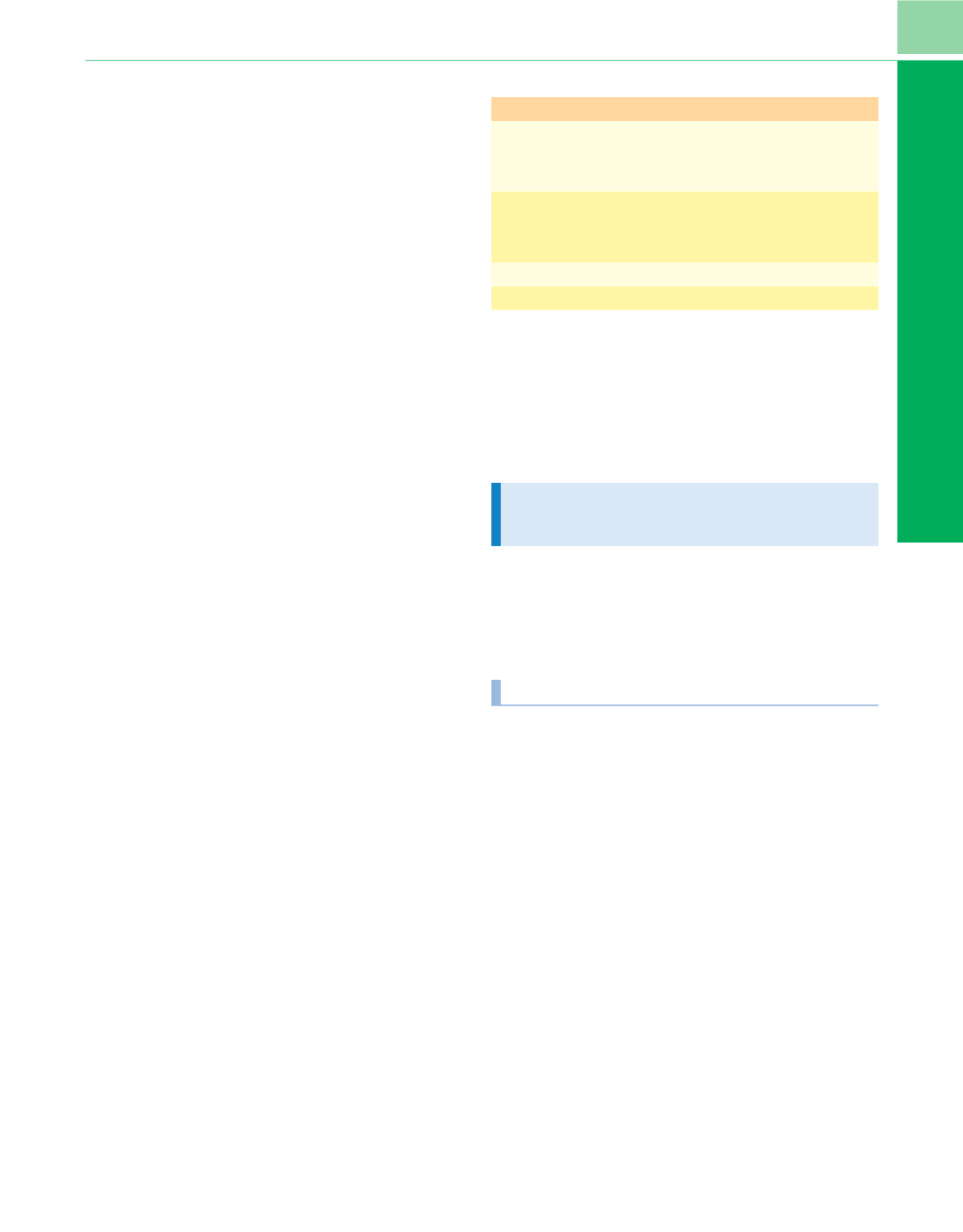
trifosfato de guanidina (GTP) a GMP cíclico. El GMP cíclico tiene
dos acciones principales: la relajación del músculo liso vascular y la
supresión de la respuesta inflamatoria. También inhibe la adhesión
leucocitaria, la activación y agregación plaquetarias y la proliferación
celular. El GMPc se convierte en GMP por las fosfodiesterasas I y V.
Por tanto, la acción local del óxido nítrico se puede potenciar por la
administración de un inhibidor selectivo de la fosfodiesterasa V,
como el sildenafilo. El propio óxido nítrico se inactiva con rapidez al
unirse al hemo intracelular y a proteínas con hemo (oxihemoglobina,
oximioglobina, guanilato ciclasa, ciclooxigenasa, citocromo P
450
).
Sintasa de óxido nítrico (NOS)
La NOS presenta varios subtipos diferentes que determinan el sitio
y la función de la síntesis de óxido nítrico. La NOS constitutiva es
dependiente del calcio y de la calmodulina y libera pequeñas can-
tidades de óxido nítrico durante períodos cortos (liberación
«tónica»). La NOS constitutiva presenta dos subtipos: NOS neuro-
nal, que actúa como un neurotransmisor periférico e induce vaso-
dilatación cerebral, y NOS endotelial, que se encuentra en el
endotelio vascular y media la actividad antes adscrita al factor
relajante derivado del endotelio (EDRF). Este último es un desta-
cado modulador de la resistencia vascular sistémica y pulmonar.
En el riñón, el óxido nítrico endógeno conserva el flujo sanguíneo
hacia la corteza yuxtamedular y médula oligohémica y puede pro-
porcionar también protección endógena contra agresiones renales
isquémicas y nefrotóxica
s 74-76.
La NOS inducible es independiente del calcio y de la calmo-
dulina y se induce por citocinas, sobre todo en células inflamato-
rias (macrófagos, granulocitos), pero también en miocitos lisos
vasculares.A niveles de activación bajos, la NOS inducible aumenta
la respuesta a la infección y estimula la inflamación y la cicatriza-
ción de las heridas. En sepsis graves, la NOS inducible produce
grandes cantidades de óxido nítrico durante períodos prolongados
(liberación «fásica») y es responsable en gran medida de la intensa
vasodilatación sistémica característica que es refractaria a la nora-
drenalin
a 77 .Los niveles elevados de óxido nítrico y sus productos
reactivos dióxido de nitrógeno y peroxinitrito inducen la peroxi-
dación lipídica y la desnaturalización de proteínas, lo que dirige el
síndrome de respuesta inflamatoria sistémica (SRIS) y la lesión
renal aguda asociada.
Dualidad del óxido nítrico en la función y la lesión
renales
Goligorsky y cols
. 78han formulado la hipótesis de que el desequi-
librio entre la expresión y la actividad de la NOS constitutiva y de
la inducible desempeña un destacado papel en la fisiopatología
de la insuficiencia renal aguda. En modelos experimentales de
sepsis, los inhibidores no selectivos de ambas formas de NOS
mejoran la presión arterial, pero empeoran la perfusión global,
incluida la renal. Los inhibidores selectivos de la NOS inducible se
muestran prometedores a la hora de suprimir la inflamación y
vasodilatación intensas a la vez que mantienen la perfusión tónica
a órganos vitales, incluidos los riñone
s 79.
Sistema de adenosina renal
Receptores de adenosina
La adenosina, el producto de degradación endógena del ATP, se
produce en todos los tipos celulares de los mamíferos y se le suele
ver como un potente vasodilatador. Sin embargo, en el riñón des-
empeña un papel esencial en la regulación del flujo sanguíneo
intrarrenal al inducir vasoconstricción en la corteza externa y con-
servar la perfusión yuxtamedular. Esta variación en su función se
explica por la identificación de al menos cuatro subtipos de recep-
tor de adenosina: A
1
, A
2a
, A
2b
y A
3
( tabla 8-3). La activación del
receptor A
1
induce vasoconstricción cortical externa; también
reduce la liberación de renina e inhibe la diuresis y la natriuresis.
Por el contrario, los receptores A
2a
aumentan el flujo sanguíneo
medular renal y estimulan la liberación de renina, la diuresis y la
natriuresis.
Lesiones isquémicas
y nefrotóxicas perioperatorias
En esta sección se revisarán situaciones y fármacos perioperatorios
que pueden alterar la fisiología renal normal. Si la alteración es lo
bastante grave o se produce en personas susceptibles, puede inducir
necrosis tubular aguda isquémica o nefrotóxica, la forma más
común de lesión aguda renal perioperatoria.
Patogénesis
Lesión por isquemia-reperfusión
En muchas situaciones clínicas (p. ej., shock hipovolémico, pinza-
miento aortico suprarenal) el riñón está sometido a una lesión
clásica de isquemia reperfusion que comprende varias fases dife-
rente
s 80 .La lesión aguda al epitelio tubular y al endotelio vascular
inicia un rápido descenso del FG. La lesión se extiende por apop-
tosis y necrosis de las células endoteliales y epiteliales. La lesión se
estabiliza durante la fase de mantenimiento, con el inicio de la
reorganización celular que culmina con la fase de recuperación. La
fase de inicio es frecuentemente breve, por lo que la fase de exten-
sión es la mejor «ventana de oportunidad» para la intervención
terapéutica que podría revertir la lesión aguda renal. Esto enfatiza
la importancia de la detección rápida y sensible de deterioros
rápidos del F
G 27 .Lesión nefrotóxica
Los mecanismos propuestos de la lesión tubular nefrotóxica han
sido abordados previamente (v. «Equilibrio de oxígeno en el asa
gruesa ascendente medular»). El riesgo de lesión renal aguda
nefrotóxica está exponencialmente relacionado con el número de
procesos nefrotóxico
s 13. Una nefrotoxina aislada (p. ej., radiocon-
traste yodado) es poco probable que cause una lesión aguda renal
cuando el riñón está bien perfundido. En los modelos animales
de necrosis tubular aguda, la inyección de radiocontraste lesión de
modo predecible más del 50% del asa gruesa ascendente medular
Fisiología renal
231
8
Sección I
Fisiología y anestesia
© ELSEVIER. Fotocopiar sin autorización es un delito
Tabla 8-3
Subtipos y funciones de los receptores de adenosina
Receptor Función agonista
Lesión isquémica
A
1
Vasoconstricción de la corteza externa Muy protectora
Disminución de la liberación de renina
Inhibición de la diuresis y la natriuresis
A
2a
Vasodilatación yuxtamedular
Muy protectora
Mayor liberación de renina
Estimulación de la diuresis y la natriuresis
A
2b
Desconocida
A
3
Desconocida
Potencia la lesión
De Fozard JR, Hann n JP: Adenosine receptor ligands: potential as therapeutic
agents in asthma and COPD.
Pulm Pharmacol Ther
12:111-114, 1999.









