
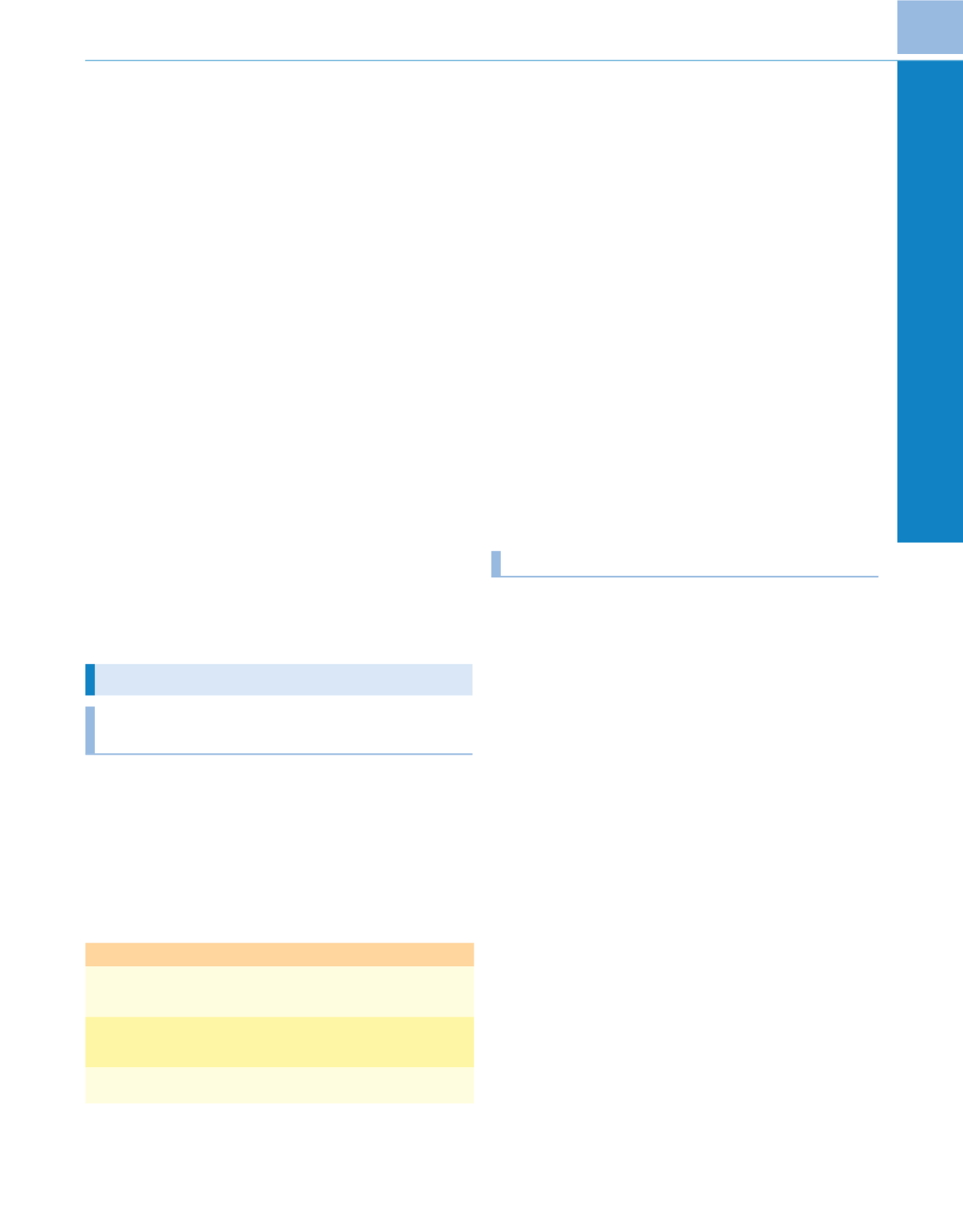
a la luz y de reflejos corneales, oculocefálicos, oculovestibulares,
orofaríngeos y respiratorios.
La irreversibilidad de la muerte cerebral puede determinarse
cuando la causa del coma es suficiente para explicar la pérdida de
función cerebral y cuando se excluye la posibilidad de recuperación
mediante observación clínica y/o pruebas complementarias. Las
pruebas complementarias que deben considerarse son análisis de
sangre y orina en busca de sustancias tóxicas, EEG, gammagrafías
cerebrales, angiografías cerebrales y potenciales evocados del
tronco encefálico. Estas pruebas de laboratorio son complementa-
rias a la historia clínica y la exploración física. Se debe descartar
cualquier factor que pueda simular los criterios clínicos o de labo-
ratorio de ausencia de función cerebral (temperatura central
<
30 °C y niveles elevados de barbitúricos en sangre). Tanto la hipo-
termia como la presencia de barbitúricos pueden deprimir de
forma significativa la actividad eléctrica en el cerebro, dando como
resultado un EEG que no se pueda interpretar. En estos casos, re
sultan útiles las angiografías isotópicas con tecnecio 99m (Tc
99m
),
que demostrarán la presencia o la ausencia de flujo sanguíneo
cerebral. Los pacientes con muerte cerebral no tienen flujo en las
arterias cerebrales anterior y media ni flujo venoso en el seno
longitudinal; el flujo sanguíneo a los tejidos extracerebrales suele
estar conservado. Este estudio es independiente de la temperatura
central del paciente o del nivel de barbitúricos. Antes de interrum-
pir las medidas de soporte, resulta útil que concurran al menos dos
médicos en el diagnóstico clínico o mediante pruebas complemen-
tarias de muerte cerebral, o en ambos. Todas las pruebas de la
muerte cerebral y las discusiones relacionadas deben documen-
tarse con claridad en la historia clínica del paciente.
Siempre que se declara la muerte cerebral de un enfermo, se
debe comentar a la familia la posibilidad de la donación de órganos.
La donación de tejidos (p. ej., oculares y válvulas cardíacas) también
es posible tras la muerte. Las agencias regionales de aprovisiona-
miento pueden facilitar protocolos y apoyo al personal de la UCI,
así como a las familias.
Sistema renal
Desarrollo estructural y funcional
del sistema excretor
El desarrollo embriológico del sistema renal comienza hacia la mitad
de la tercera semana de la gestación, con la aparición del túbulo
pronefrítico. Hacia la semana 10 de la gestación, existe un riñón y
un sistema colector funcionantes y la orina del feto es eliminada a
la vejiga. Entre las 32 y las 36 semanas de gestación está presente
la dotación completa de nefronas de cada riñón. La
tabla 74-9presenta los valores normales de la función renal pediátrica.
Desarrollo funcional del riñón
Como la placenta es el principal órgano excretor del feto, el creci-
miento renal no es dirigido por requerimientos funcionales. El
crecimiento renal en el tercer trimestre aumenta de forma lineal
con el peso y la superficie corporales. La tasa de filtrado glomerular
(FG) aumenta con rapidez desde la semana 28 a la 35 de la gesta-
ción. En los nacidos a término, el FG es de 10ml/min/m
2
, y aumenta
hasta los 20ml/min/m
2
hacia las 2 semanas de vida. Aunque el FG
es menor en los lactantes prematuros, el ritmo de aumento es el
mismo que en los nacidos a términ
o 162 .Las funciones tubulares no
se encuentran completamente maduras en los recién nacidos a
término. El riñón del neonato es sensible a la hormona antidiuré-
tica (ADH) y a la vasopresina, pero la osmolaridad de la orina
puede variar desde sólo 50 hasta 780mOsm/
l 163 .La función tubular
de los lactantes prematuros es menos madura.
El umbral renal para el bicarbonato en el neonato se acerca
a 20mEq/l, lo que significa que los normogramas acidobásicos
habituales no pueden aplicarse a los lactantes, ya que su concentra-
ción de bicarbonato sérico de 20mEq/l no indica acidosis metabó-
lica. El umbral tubular renal para la glucosa se encuentra a niveles
de adulto en los lactantes a término, pero en los lactantes prematu-
ros es tan sólo de 125-150mg/dl. Los lactantes a término poseen
una excreción fraccionada de sodio del 1% o menor hacia el tercer
día de vida. La excreción fraccionada de sodio puede ser mucho
mayor (5%) en lactantes prematuro
s 164. Los niveles de renina, angio-
tensina y aldosterona se encuentran elevados en el recién nacido y
se reducen a lo largo de las primeras semanas de vida. La
tabla 74-9presenta los valores normales de la función renal pediátric
a 165.
Insuficiencia renal
La insuficiencia renal aguda se define como la pérdida brusca y a
menudo temporal de función renal
(v. caps. 55 y 57). La oliguria es
la regla, la poliuria la excepción y la anuria resulta infrecuente. El
volumen y la composición urinarios se ven alterados y con frecuencia
se asocian trastornos de los líquidos, los electrólitos y acidobásicos.
El tratamiento va encaminado al mantenimiento de una homeostasis
normal del metabolismo y de los líquidos, manteniendo la nutrición
y con paciencia. La insuficiencia renal aguda puede estar causada por
trastornos prerrenales, posrenales (obstructivos) o renales intrínse-
cos. Las causas prerrenales se relacionan con la disminución del flujo
sanguíneo. La reducción del gasto cardíaco o del flujo sanguíneo
renal son causas frecuentes de disminución de la producción de orina
y acaban causando azoemia y daño renal isquémico. La adecuación
del volumen sanguíneo circulante se valora mediante la PVC y la
determinación del gasto cardíaco y la evaluación del flujo sanguíneo
renal mediante estudios de flujo con Doppler o mediante técnicas de
medicina nuclear. Estos estudios resultan útiles a la hora de distinguir
las causas prerrenales de las renales de azoemia, pero pueden ser
difíciles de realizar en los neonatos enfermos.
La obstrucción posrenal del flujo de orina puede ocurrir en
cualquier lugar del sistema colector, pero es más frecuente en forma
de obstrucción parcial a nivel del cuello de la vejiga o en la unión
ureterovesical o ureteropélvica. Todas estasmalformaciones pueden
provocar una nefropatía obstructiva y daño renal o insuficiencia
renal. Los signos de obstrucción pueden ser sutiles y precisar de
una evaluación radiológica, ecográfica o endoscópica. Las infeccio-
nes recurrentes del tracto urinario son con frecuencia la manifes-
tación clínica de lesiones obstructiva
s 166 .La insuficiencia renal intrínseca puede deberse a trastornos
de los glomérulos renales, de los túbulos o de los vasos sanguíneos.
Entre las enfermedades glomerulares se encuentran el síndrome
hemolítico-urémico (SHU), la glomerulonefritis postestreptocó-
cica, la púrpura de Schönlein-Henoch y otras enfermedades infla-
matorias y por inmunocomplejos. La lesión tubular aguda está
Cuidados intensivos pediátricos y neonatales
2441
74
Sección V
Anestesia pediátrica
© ELSEVIER. Fotocopiar sin autorización es un delito
Tabla 74-9
Valores normales de la función renal pediátrica
Edad
Valor
Creatinina (mg/dl)
1 año
10 años
18 años
0,41±0,1
0,61±0,22
0,91±0,17
Filtrado glomerular
(ml/min/1,72 m
2
)
2-8 días
6-12 meses
2-12 años
39 (rango, 17-60)
103 (rango, 49-157)
127 (rango, 89-165)
Concentración de la
orina (mOsm/l)
1 mes
2-16 meses
600-1.100
1.089 (rango, 870-1.309)
Modificada de Goldsmith DI: Clinical and laboratory evaluation of renal function.
En
Edelman CM Jr (ed.):
Pediatric Kidney Disease
. Boston, Little, Brown, 1978, pág. 213.









