
Aunque la incidencia de insuficiencia hepática es baja, la mayoría
de los pacientes con hepatitis por halotano tienen anticuerpos
frente a las proteínas modificadas por TFA. Esto implica que la
modificación de la proteína por el metabolito reactivo ha pro-
ducido la respuesta inmunitaria. Además, muchos pacientes tienen anticuerpos frente a las proteínas nativas. Los pacientes
con frecuencia tienen antecedentes de exposiciones múltiples a
la anestesia con halotano y uno o más síntomas de procesos
inmunológicos activos como fiebre, exantema, artralgias y eosi-
nofili
a 90-98 .No hay datos de que estos anticuerpos que se obser-
van en la hepatitis por halotano medien la lesión hepática; es
muy posible que sean sólo marcadores de la respuesta inmuno-
lógica. Parece que los complejos TFA-proteína
( tabla 14-3) pro-
ducidos por el metabolismo oxidativo del halotano, inducen una
respuesta citotóxica de linfocitos T en individuos sensibilizados
que en posteriores exposiciones producen hepatitis por halotano
( fig. 14-13 ) 99,100 .Hepatitis por halotano en pacientes pediátricos
El primer caso de hepatitis por halotano en un niño se describió
en 195
9 101 .Desde entonces ha habido muchas comunicaciones de
hepatotoxicidad y necrosis hepática masiva después de la aneste-
sia con halotano en niños (v. también cap. 72). En dos estudios
retrospectivos se analizó la incidencia de hepatotoxicidad por
halotano en niños. En el primero se estudiaron 165.400 niños
anestesiados con halotano en un hospital infantil en el Reino
Unido entre 1957 y 1979, y se encontró una incidencia de 1 por
82.00
0 102. En el segundo estudio se analizaron 200.311 casos entre
1958 y 1983 en un hospital infantil en Estados Unidos. Sólo se
encontró un paciente con hepatitis por halotan
o 103 .En 1987,
se describieron siete casos de niños entre los 11 meses y los
15 años de edad con hepatitis por halotano, todos ellos anestesia-
dos en más de una ocasió
n 104 .El diagnóstico en este estudio se
confirmó en todos los casos menos en uno por la presencia de
anticuerpos séricos que reaccionaban con antígenos de hepato-
cito alterados por halotano. Un paciente murió, y los investigado-
res excluyeron otras causas de hepatopatía. Estos hallazgos
indican que la hepatitis por halotano puede aparecer antes de la
pubertad, aunque es menos frecuente que en adultos. No está
claro el motivo de esta diferencia de incidencias observada entre
adultos y niños, ya que se ha descubierto que el halotano se meta-
boliza en grados parecidos en adultos y en niños y existe inmu-
nocompetencia desde el nacimiento.
Enflurano, isoflurano, desflurano y sevoflurano
La incidencia de lesión hepática por anestésicos inhalatorios
fluorados sigue el orden siguiente: halotano
>
enflurano
>
iso-
flurano
>
desflurano, y se corresponde con el grado de metabo-
lismo oxidativo de cada uno de ellos
( fig. 14-8 ), que es halotano
(
≈
20%), enflurano (
≈
2,5%), isoflurano (
≈
0,2%) y desflurano
(
≈
0,01%
) 105 .Dado que todos estos anestésicos inhalatorios
parecen formar complejos de inclusión proteicos idénticos o
relacionados en su estructura con los del halotano, parece posible
que produzcan lesión hepática por un mecanismo similar al de
este, aunque con una incidencia considerablemente más baja
( fig. 14-14). Esta incidencia más baja puede ser debida a la
menor concentración de complejos de proteínas potencialmente
inmunógenos formados por estos fármacos en comparación con
el halotano cuando sufren metabolismo oxidativo por la CYP2E1
( fig. 14-15).
El enflurano se utilizó por primera vez en Norteamérica en
1966. Aunque en la actualidad se usa mucho menos, durante el
período de empleo más alto hubo relativamente pocos casos de
lesión hepática relacionados con él. En 1986, Eger y cols. revisa-
ron 10 comunicaciones publicadas y varios informes no publica-
dos de lesión hepática después de la administración de enflurano.
En muchas de estas historias faltaban datos fundamentales como
la duración de la exposición anestésica, la confirmación histoló-
gica de lesión hepática y la exposición previa a hepatopatía o
fármacos hepatotóxicos. Además, varios pacientes habían sufrido
hipotensión o afectación grave o demostraron signos de shock y
se sometieron a intervenciones con potencial conocido para dis-
función hepática. A los investigadores no les quedó otra opción
que concluir que las pruebas no apoyaban la existencia de dis-
función hepática producida por el enflurano similar a la obser-
vada con el halotano. Sin embargo, varias comunicaciones indican
que la anestesia con enflurano puede producir hepatotoxicidad
en pacientes previamente anestesiados con halotano o sensibili-
zados a él. Se demostró que los complejos de proteínas de halo-
tano y enflurano formados en el hígado de ratas tratadas con
estos dos fármacos por separado reaccionaban con anticuerpos
séricos de pacientes diagnosticados de hepatitis por halotan
o 106 .Esta reactividad cruzada aparente puede explicarse por la simili-
412
Farmacología y anestesia
II
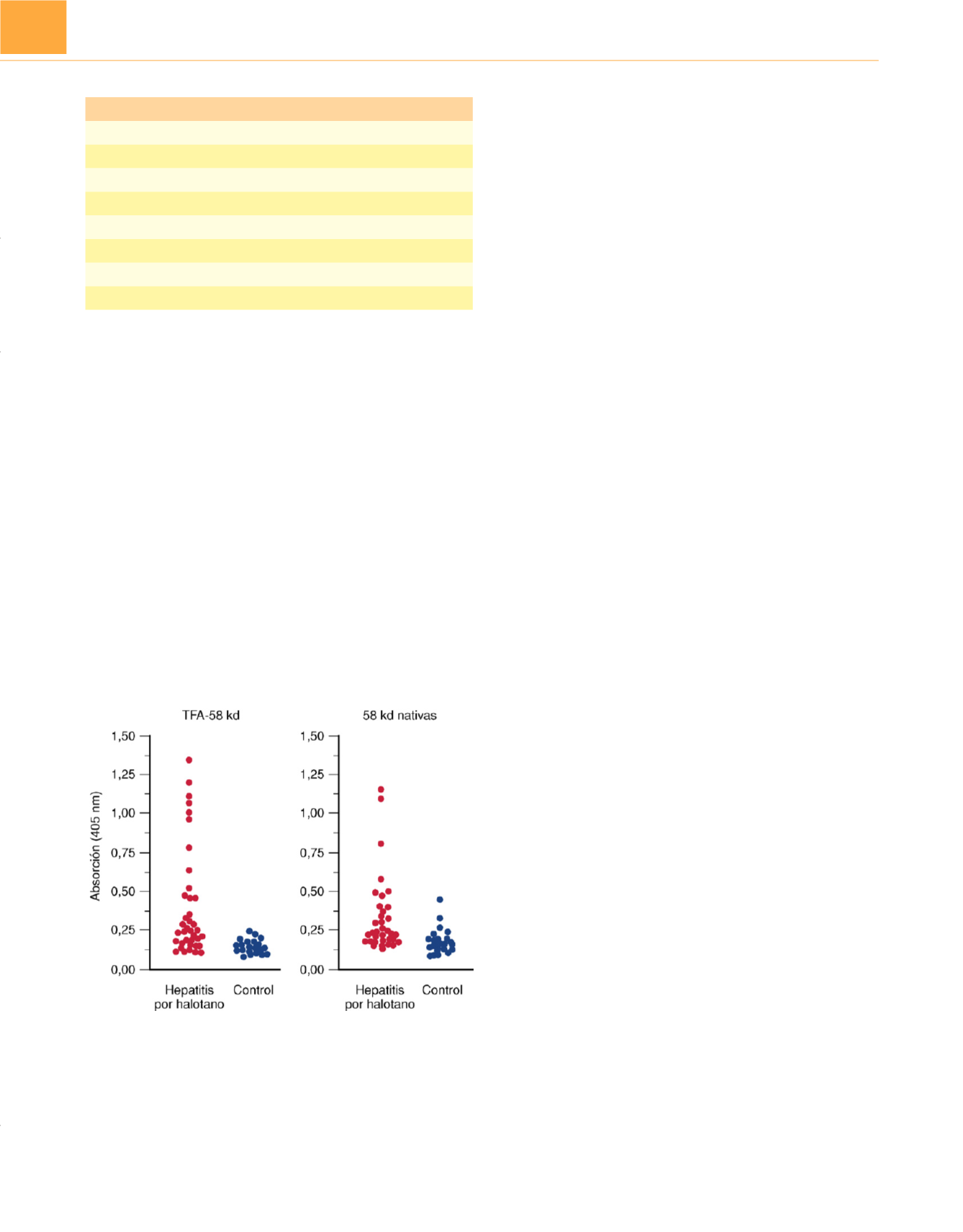
Figura 14-13
Prueba de inmunotransferencia en sueros de pacientes con
hepatitis por halotano para anticuerpos que reaccionen con proteínas
trifluoroacetiladas y nativas de 58 kd. Todos los sueros de los 40 pacientes con
hepatitis por halotano y 32 control se analizaron a una dilución de 1:100.
(Adaptada de Martin JL, Reed GF, Pohl LR: Association of anti-58 kDa
endoplasmic reticulum antibodies with halothane hepatitis.
Biochem
Pharmacol
46:1247-1250, 1993.)
Tabla 14-3
Antígenos del halotano
Peso molecular (kd)
Proteína
100
Endoplasmina
82
GRP-78
80
ERP-72
63
Calreticulina
59
Carboxilesterasa
58
Proteín disulfuro isomerasa (isoforma)
57
Proteín disulfuro isomerasa
54
Citocromo P450









