
sintetasa del ácido
g
-aminolevulínico, que es la enzima responsable
de la producción de las porfirina
s 183 .Como ya se ha mencionado antes, el metabolismo hepático es
responsable de la eliminación de todos los barbitúricos, excepto del
fenobarbital. La excreción renal es importante en la eliminación de
este fármaco, con un 60-90% del mismo que se elimina por esta vía,
sin ser modificado. De los otros barbitúricos sólo una pequeña can-
tidad es excretada sin modificar por el riñón. La alcalinización de la
orina con bicarbonato favorece la excreción renal del fenobarbital.
El metohexital se metaboliza en el hígado mediante la oxidación
a un alcohol; también se produce
N
-desalquilación.Cuando se compara
con el tiopental, el metohexital tiene una semivida de eliminación, un
volumen de distribución,y una unión a proteínas similares a éste.Existe
una diferencia significativa en la desaparición plasmática y en la semi-
vida de eliminación (4 horas para el metohexital y hasta 12 horas para
el tiopental). Esta diferencia se debe a que el aclaramiento hepático del
metohexital es tres veces más rápido, con una velocidad media de 7,8-
12,5ml/kg/mi
n 184. La tasa de extracción hepática del metohexital (acla-
ramiento/flujo sanguíneo hepático) es de alrededor de 0,5,lo que indica
que el hígado extrae el 50%del fármaco que pasa por él.Por el contrario,
la tasa de extracción hepática del tiopental es inferior (0,15).
Farmacocinética
La farmacocinética de los barbitúricos ha sido descrita como un
modelo fisiológico y como unmodelo compartimental. En los últimos
años, este último modelo ha sido el que más apoyos ha recibid
o 185 .Los
modelos fisiológicos de los barbitúricos describen una mezcla rápida
del fármaco con el volumen sanguíneo del compartimento central, y
más tarde una distribución rápida del fármaco a los tejidos muy per-
fundidos, de volumen bajo (es decir, el cerebro), y una redistribución
más lenta a los tejidos magros (músculo), que pone fin al efecto de la
dosis de inducción. En estos modelos, la captación del fármaco por el
tejido adiposo y el aclaramientometabólico (eliminación) sólo desem-
peñan un papel poco relevante en el final del efecto de la dosis de
inducción,debido a la baja perfusión en comparación con otros tejidos
y a la eliminación lenta, respectivamente. Los valores del modelo
compartimental del tiopental y del metohexital, los barbitúricos que
más se utilizan para la inducción, se pueden ver en la
tabla 16-1 .Ambos modelos describen una rápida redistribución como
principal mecanismo que finaliza el efecto de una dosis de inducción
única. El modelo compartimental explica el retraso en la recuperación
después de una infusión continua. Este modelo describe el fenómeno
por el cual el fin del efecto es altamente dependiente de la lentitud del
proceso de captación en el tejido adiposo y de la eliminación o acla-
ramiento por el metabolismo hepático. Después de una infusión pro-
longada, la farmacocinética del metabolismo de los barbitúricos es
más parecida a un metabolismo no lineal de Michaelis-Menten.
Cuando se utilizan las dosis habituales (4-5mg/kg), el tiopen-
tal muestra una cinética de primer orden (es decir, una
fracción
constante del fármaco se elimina del organismo por unidad de
tiempo); sin embargo, si se utilizan dosis de tiopental más altas (300-
600mg/kg), se saturan los receptores, y sigue una cinética de orden
cero (es decir, una
cantidad
constante del fármaco se elimina por
unidad de tiempo). El volumen de distribución es algo mayor en las
mujeres que en los varones, de ahí que la semivida de eliminación
sea mayor en las mujere
s 186. El embarazo también aumenta el
volumen de distribución del tiopental, y por tanto alarga la semivida
de eliminació
n 187 .Como se ha señalado antes, el aclaramiento del
tiopental no se ve alterado en pacientes con cirrosis, pues la cantidad
de proteínas disponibles para que el fármaco se una a ellas es sufi-
ciente, incluso en estadios avanzados de la enfermeda
d 188 .Debido a la afinidad de este fármaco por la grasa, al volumen
de distribución relativamente grande y al escaso aclaramiento
hepático, el tiopental se puede acumular en los tejidos, sobre todo
si se administran dosis grandes o durante períodos prolongados de
tiempo. El nivel plasmático del fármaco aumenta cuando se admi-
nistraban dosis repetidas del mism
o 189 .El diseño de esquemas de
infusión adecuados asegura la obtención de niveles sanguíneos
constantes y que se mantenga el efecto hipnótico, aunque no se
utilizan en la práctica clínica habitual.
Farmacología
Mecanismo de acción
Se han realizado numerosas investigaciones para aclarar el mecanismo
deaccióndelosbarbitúricosenelSNC;sinembargo,conlaexcepciónde
su efecto en el receptor GABA
A
, el modo de acción se desconoce
todaví
a 190-191 .Diversos estudios recientes han empezado a dilucidar el
papel de los receptores NMDA en la acción de los barbitúrico
s 192-195 .El efecto específico de los barbitúricos en la neurofisiología del SNC
se ha agrupado en dos grandes categorías: 1) potenciación del efecto
en la sinapsis de los neurotransmisores
inhibidores
y 2) bloqueo del
efecto en la sinapsis de los neurotransmisores
excitadore
s 196.
El GABA es el principal neurotransmisor inhibidor en el SNC
de los mamíferos, y el receptor GABA
A
es el único sitio cuya implica-
ción en la anestesia inducida por los barbitúrico
s 191ha sido demos-
trada. El receptor GABA
A
es un canal del ion cloro, formado al menos
por cinco subunidades con sitios de acción específicos para el GABA,
los barbitúricos, las benzodiazepinas y otras molécula
s 179. La unión de
un barbitúrico al receptor GABA
A
potencia, por un lado, el efecto del
GABA y, por otro, reproduce el efecto de éste, y aumenta el transporte
496
Farmacología y anestesia
II
Figura 16-5
Formas tautómeras ceto y enol del ácido barbitúrico; se han
identificado los sitios de sustitución de los barbitúricos hipnóticamente
activos como 1, 2 y 5.
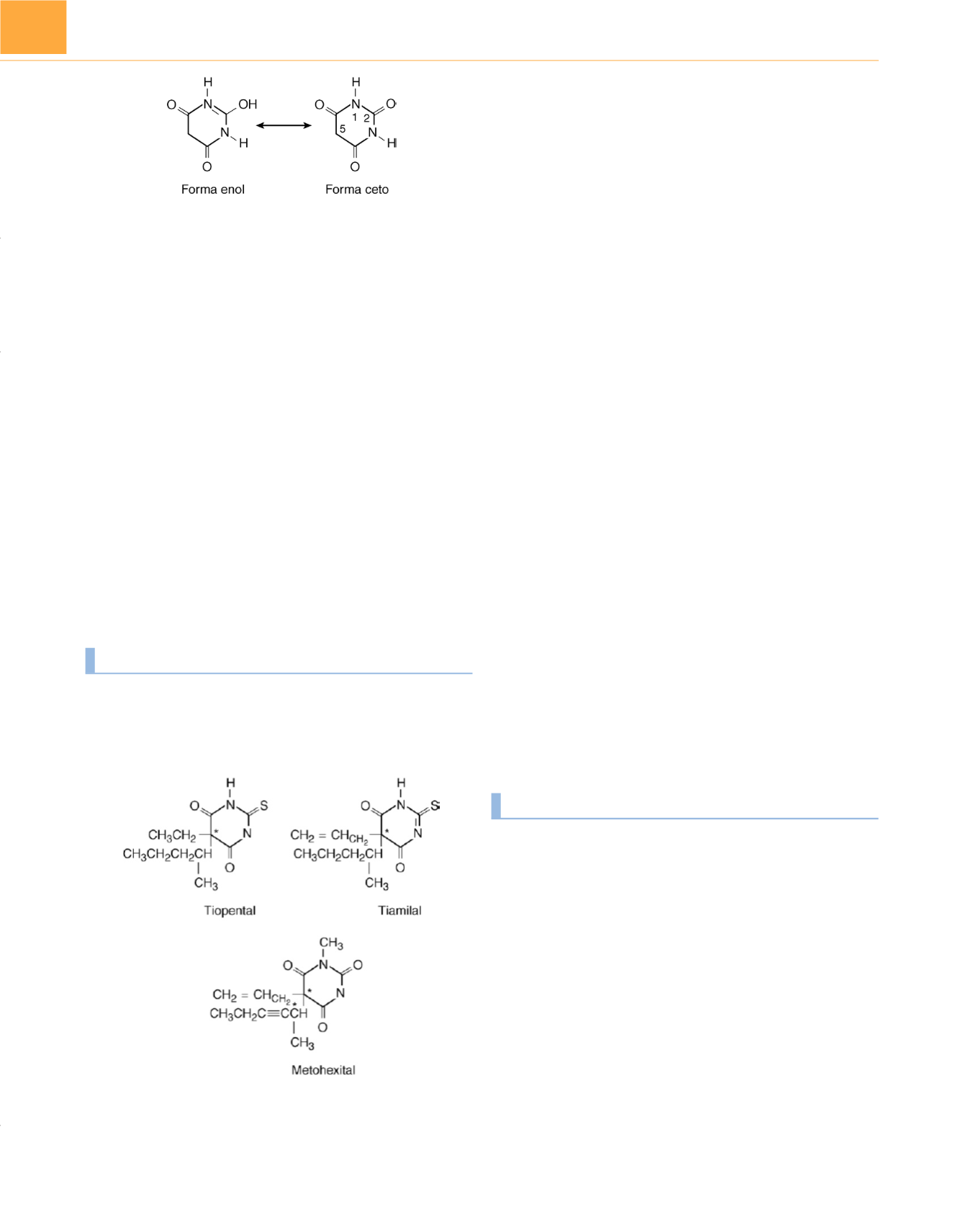
Figura 16-6
Barbitúricos con propiedades hipnóticas usados a menudo para
la inducción; los asteriscos marcan los centros asimétricos.









