
suficientemente altas como para alterar el rendimiento del personal
de quirófano y reducir su vigilancia.
El método más sencillo para reducir la pérdida cutánea de
calor es aplicar aislamiento pasivo a la superficie cutánea. Los
aislantes fácilmente disponibles en la mayoría de los quirófanos
son mantas de algodón, paños quirúrgicos, láminas de plástico y
compuestos reflectores («mantas espaciales»). Una única capa de
cada uno de ellos reduce la pérdida de calor aproximadamente un
30%, sin diferencias clínicas significativas entre los tipos de aisla-
miento. La reducción de la pérdida de calor es similar en todos los
aislantes pasivos de uso habitual, porque el aislamiento lo propor-
ciona en su mayor parte la capa de aire inmóvil atrapada bajo la
cubierta. Por consiguiente, añadir más capas de aislante reduce
sólo ligeramente la pérdida de calor. Por ejemplo, una manta de
algodón reduce la pérdida de calor un 30%, mientras que tres
mantas de algodón la reducen sólo un 50%. Además, el calenta-
miento de las mantas de algodón proporciona un beneficio escaso
y de poca duració
n 146 .Estos datos indican que la simple adición de
más capas de aislante pasivo o el calentamiento del aislante antes
de su aplicación serán, por lo general, insuficientes en pacientes
que desarrollen hipotermia mientras están cubiertos con una sola
capa de aislante.
La pérdida cutánea de calor es aproximadamente proporcio-
nal a la superficie corporal tota
l 147. (La creencia popular de que
gran parte del calor metabólico se pierde por la cabeza es falsa en
adultos. Esta pérdida puede ser sustancial en pequeños lactante
s 148 ,pero es mayor, sobre todo, porque la cabeza representa una gran
parte de la superficie corporal total.) Por tanto, la cantidad de piel
cubierta es más relevante que aislar determinadas partes del cuerpo.
No tiene sentido, por ejemplo, cubrir la cabeza y dejar los brazos
expuestos; los brazos tienen más superficie que la cabeza y produ-
cirían mayor pérdida de calor.
El simple aislamiento pasivo pocas veces es suficiente para
mantener la normotermia en pacientes sometidos a grandes inter-
venciones; en estos casos se requiere calentamiento activo. Dado
que el 90% del calor metabólico se pierde a través de la superficie
de la piel, sólo el calentamiento cutáneo transferirá suficiente calor
para evitar la hipotermia. Por consiguiente, para un uso intraope-
ratorio, el agua circulante y el aire forzado son los dos sistemas
principales que deben considerarse.
Varios estudios han descrito de manera sistemática que los
colchones de agua circulante son casi ineficace
s 149 .Se supone que
son incapaces de mantener la normotermia porque se pierde poco
calor desde la espalda hacia los 5 cm de espuma aislante que recu-
bren la mayoría de las mesas de quirófano. Además, la combina-
ción de calor y disminución de la perfusión local (producida por
la reducción del flujo sanguíneo capilar debida al peso del paciente)
incrementa la tendencia a la necrosis por presión/calor («quema-
duras»). Tal lesión tisular puede ocurrir incluso cuando la tempe-
ratura del agua no sobrepase los 40 °
C 150 .El agua circulante es más
eficaz (y más segura) cuando se coloca
sobre
los pacientes que
bajo
ellos y, en esa posición, puede eliminar casi por completo la pérdida
metabólica de calor. La producción metabólica de calor aumentará
la temperatura corporal media aproximadamente 1 °C/h cuando
se elimine la pérdida de calor. Las prendas con agua circulante
recientemente diseñadas transfieren grandes cantidades de calor
al aumentar la superficie calentada o al usar materiales que facili-
tan la conducció
n 151,152 .El sistema perianestésico de calentamiento más habitual es
el aire forzado. Los mejores sistemas de aire forzado eliminan por
completo la pérdida de calor de la superficie cutáne
a 123 .El aire
forzado suele mantener la normotermia incluso durante las inter-
venciones más extensa
s 56y es mejor que los colchones de agua
circulant
e 153 .Asimismo, es notablemente más seguro; son escasas
las lesiones descritas con el uso correcto.
Inducción de hipotermia terapéutica
moderada
Los datos que apoyan la aplicación de la hipotermia terapéutica en
otras indicaciones aparte de la parada cardíaca y el neonato con
asfixia son escasos, a pesar de lo cual esta técnica se utiliza ocasional-
mente durante la neurocirugía o el infarto de miocardio agudo. Nor-
malmente se buscan temperaturas centrales de 32-34°C y se piensa
que es importante alcanzar con rapidez la temperatura buscada.
El enfriamiento pasivo es demasiado lento para la inducción
de la hipotermia terapéutica. La inmersión en agua fría es el método
no invasivo más rápido para enfriar activamente a los pacientes, si
bien es difícil de conseguir en las condiciones clínicas y supone un
riesgo sustancial de seguridad eléctrica. La administración de líqui-
dos intravenosos refrigerados también es eficaz y reduce la tempera-
tura corporal en 0,5°C/
l 154, pero su uso no es posible en los pacientes
neuroquirúrgicos, en los que se deben restringir los líquidos.
El enfriamiento por aire forzado es fácil de realizar, pero
relativamente lento; se necesitan aproximadamente 2,5 horas para
enfriar a los pacientes neuroquirúrgicos hasta 33 °
C 134 .Es poco
probable que los colchones de agua circulante convencionales sean
eficaces, debido a la relativamente escasa superficie cutánea en
contacto con el colchón y a que el propio peso corporal del paciente
reduce la convección sanguínea de calor a la espalda. Los nuevos
sistemas de agua circulante incluyen cubiertas a modo de prenda
o las «almohadillas para intercambio de energía», que cubren
mucha más superficie cutánea y transfieren grandes cantidades de
calor, por lo que son bastante eficace
s 155 .La mejor forma de inducir una hipotermia terapéutica
rápida tal vez sea la refrigeración endovascular. Estos sistemas con-
sisten en un catéter intercambiador de calor, habitualmente inser-
tado en la vena cava inferior a través de la vena femoral, y un
servocontrolador. Pueden reducir las temperaturas centrales a
ritmos cercanos a 4 °C/h
( fig. 38-18 ) 156 .La inducción de hipotermia terapéutica durante la cirugía es
relativamente fácil, porque los anestésicos alteran profundamente
las respuestas termorreguladoras. Por el contrario, los pacientes no
anestesiados (incluso aquellos que han sufrido un ictus) defienden
vigorosamente la temperatura central mediante la vasoconstricción
Regulación y monitorización de la temperatura
1313
38
Sección III
Control de la anestesia
© ELSEVIER. Fotocopiar sin autorización es un delito
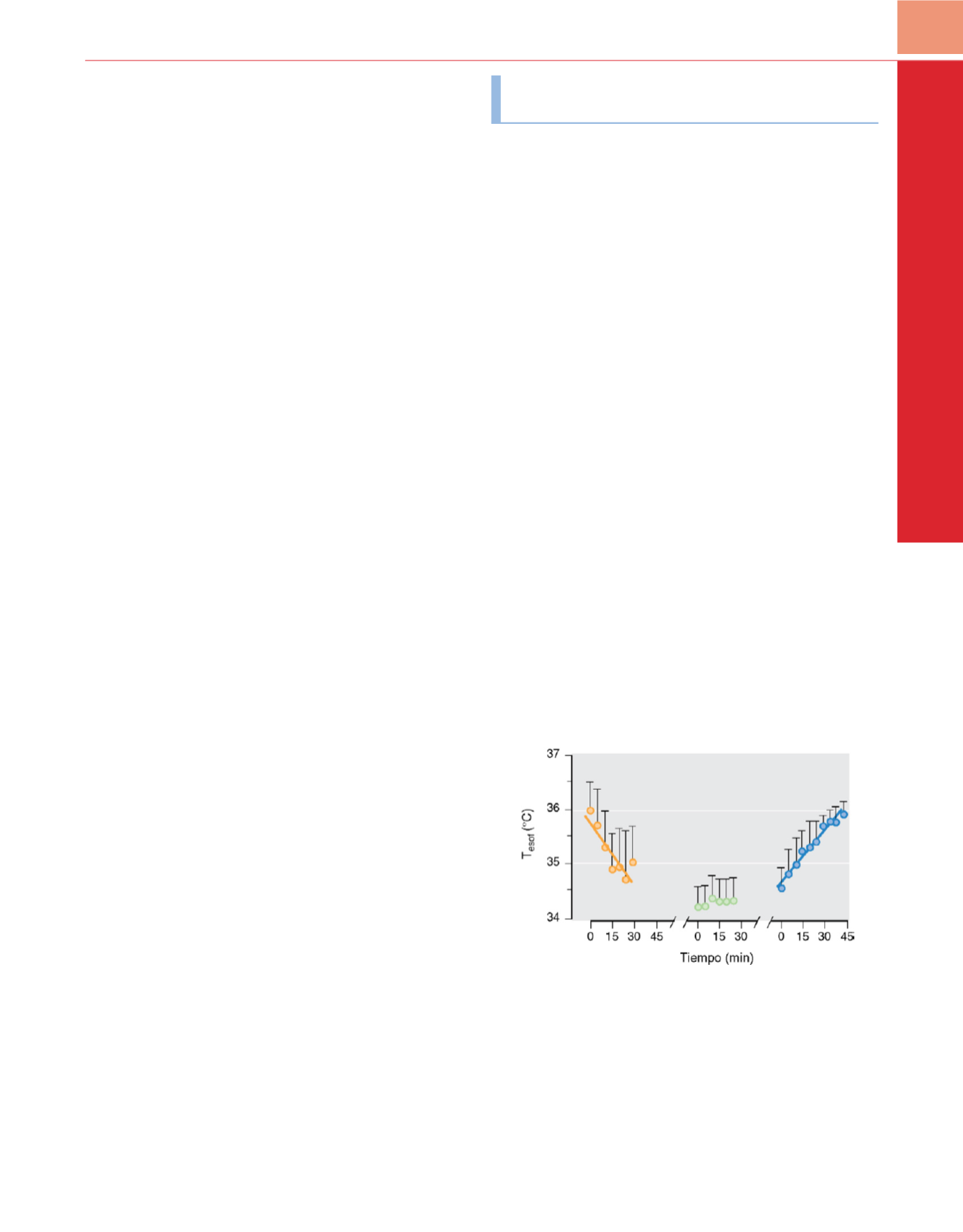
Figura 38-18
Temperaturas esofágicas (T
esof
) intraoperatorias medias (±DE)
durante los períodos de enfriamiento, mantenimiento de la temperatura y
recalentamiento en ocho pacientes neuroquirúrgicos que fueron enfriados
con catéteres endovasculares intercambiadores de calor en la vena cava. El
tiempo cero identifica el comienzo de cada período de tratamiento térmico;
la duración de estos períodos difiere en pacientes individuales, según la
duración de la cirugía y otros factores. Se muestran las líneas de regresión en
los períodos de enfriamiento y recalentamiento.
(De Doufas AG, Akça O,
Barry A y cols.: Initial experience with a novel heat-exchanging catheter in
neurosurgical patients.
Anesth Analg
95:1752-1756, 2002.)









