
durante la década de 1970. Antes del uso de los opioides, anestesiar
a los pacientes con una enfermedad valvular o congénita del corazón
sin causar colapso cardiovascular era un problema. Estos primeros
pacientes de la cirugía cardíaca estaban muy enfermos y tenían poca
o ninguna reserva circulatoria. A finales de la década de 1960,
Lowenstein y cols
. 130observaron la estabilidad hemodinámica de los
pacientes sometidos a ventilación mecánica a quienes se les admi-
nistraba con frecuencia grandes dosis de morfina por vía intrave-
nosa para suprimir la respiración en las unidades de cuidados
intensivos. Esta observación animó a Lowenstein y cols. a ser los
primeros en administrar morfina (0,5 a 3mg/kg) como el fármaco
«anestésico» único. La estabilidad cardiovascular resultante en los
pacientes con enfermedad valvular aguda adquirida del corazón era
impresionante.Cuando lametodología de la cirugía cardíaca avanzó,
se comenzó a aplicar anestesia quirúrgica a los pacientes con enfer-
medad cardíaca isquémica. Desgraciadamente, la anestesia con
morfina tenía menos éxito en estos pacientes, en los que se desarro-
llaba hipertensión, taquicardia y consciencia durante la cirugí
a 130.
En 1978, Stanley y Webste
r 131introdujeron el uso de dosis
altas de fentanilo para la anestesia cardíaca. Esta técnica minimizaba
los efectos indeseables de la morfina en la inducción (hipotensión)
y proporcionaba una mejor estabilidad hemodinámica en pacientes
con buena función ventricular y enfermedad cardíaca isquémica.
Sin embargo, cuando aumentó la experiencia clínica con el fenta-
nilo, los investigadores observaron que, aunque se elevara mucho la
dosis de fentanilo, no siempre se producía un estado anestésico
fiable, como se define en la
figura 29-7, para los estímulos más
potentes y era difícil eliminar las respuesta
s 132. Este descubrimiento
demostró que los opioides no son «anestésicos», sino sólo analgési-
cos potentes e hipnóticos débiles, como se indica en la
figura 29-2 .Muchos estudios confirman este hallazgo.Wynands y cols
. 14usaron dosis de fentanilo solo, de moderadas a grandes (50 a
150
m
g/ml), sin ningún otro fármaco anestésico (ni componentes
hipnóticos), y midieron las concentraciones plasmáticas a los estí-
mulos quirúrgicos definidos (intubación, incisión cutánea, esterno-
tomía, disección de la raíz aórtica) en pacientes con buena función
ventricular a los que se les realizó cirugía coronaria. En cerca del
20% de los pacientes, las concentraciones plasmáticas extremada-
mente altas de fentanilo (15ng/ml) no eliminaron las respuestas
hemodinámicas, definidas como un aumento del 20% de la presión
arterial sistólica. Estos resultados han sido confirmados por
Hynynen y cols
. 133y por Philbin y cols
. 134 .Murphy y Hu
g 135midieron la capacidad del fentanilo para
disminuir la CAM de enflurano en los perros. Anestesiaron primero
a los perros con enflurano y determinaron la CAM.Después utilizaron
varias infusiones de fentanilo en concentraciones progresivamente
más altas para conseguir una concentración plasmática equilibrada
constante de fentanilo en cada animal. Cada vez que se aumentaba la
concentración de la infusión, se determinaba nuevamente la CAM de
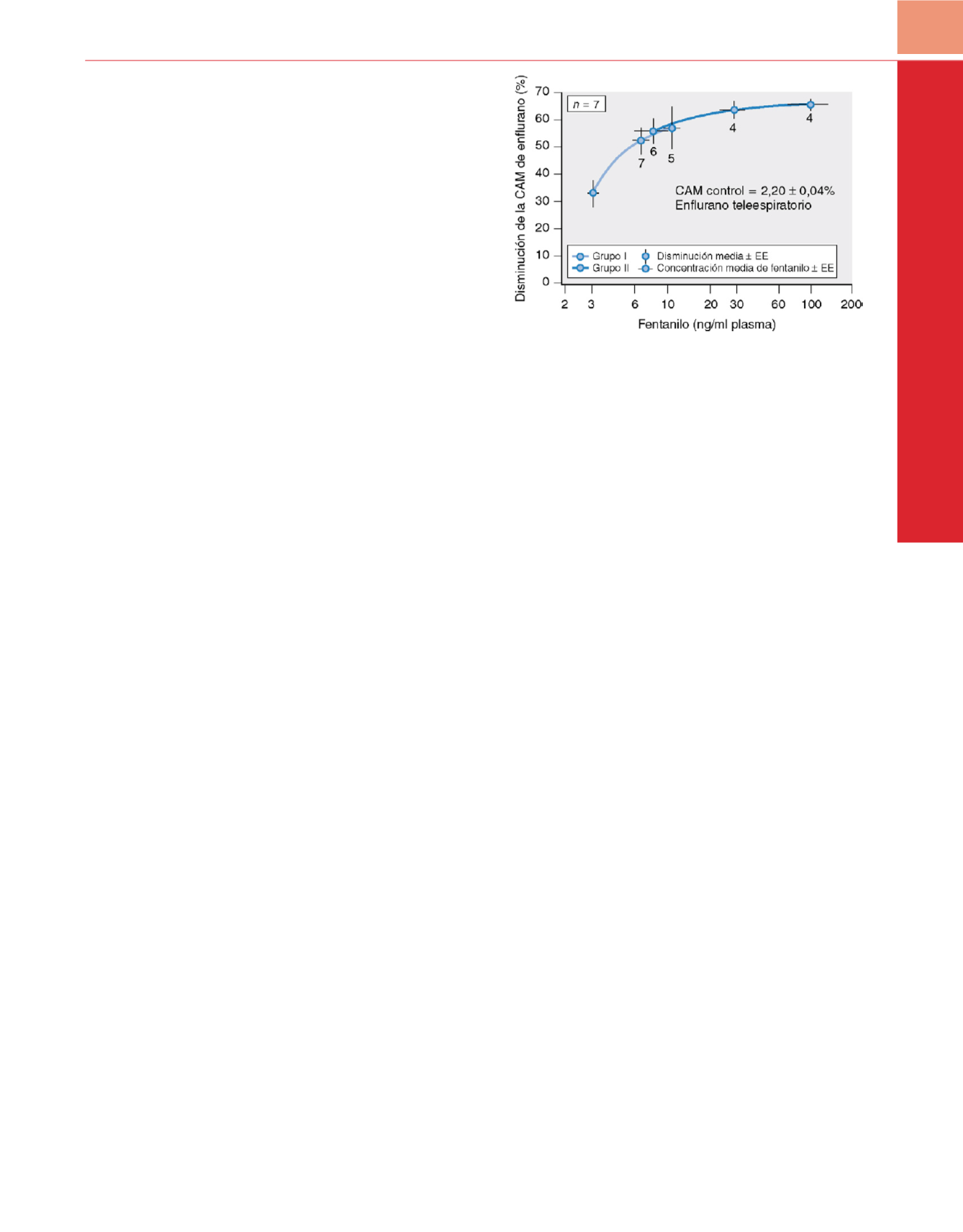
enflurano. Murphy y Hug observaron que incluso concentraciones
plasmáticas muy elevadas de fentanilo (20ng/ml) no disminuían la
CAMde enfluranomás allá del 60 al 70%de su valor inicial
( fig.29-16 ).
Es decir, existe un techo para el efecto de enflurano. La morfina, el
sufentanilo y el alfentanilo también disminuyeron la CAM del enflu-
rano y tienen un efecto techo similar en los perro
s 136–138.
McEwan y cols. emprendieron estudios similares en los
humanos y describieron la disminución de la CAM del isoflurano
con varias concentraciones plasmáticas constantes de fentanilo
medidas con una bomba de infusión controlada por ordenador
16 .Se examinó la respuesta de movimiento a la incisión cutánea inicial
respecto de las concentraciones teleespiratorias de isoflurano. Estos
investigadore
s 16encontraron en los humanos resultados muy pare-
cidos a los que observaron Hug y cols. en los perros. La CAM de
isoflurano disminuyó un 39% a concentraciones plasmáticas esta-
bles de fentanilo de 1ng/ml y un 63% a concentraciones plasmáti-
cas de fentanilo de 3ng/ml. El incremento de las concentraciones
plasmáticas de fentanilo a más de 3ng/ml producía un mínimo
aumento de la reducción de la CAM de isoflurano. La reducción
máxima de la CAM fue del 82% a concentraciones plasmáticas de
fentanilo equilibradas de 10,6ng/ml. Con otros anestésicos inhala-
torios (desflurano, sevoflurano) y otros opioides (alfentanilo, sufen-
tanilo, remifentanilo
) 6,139se obtuvieron resultados similares de la
reducción de la CAM.
Cuando se examinaron otros objetivos de los anestésicos
inhalatorios e interacciones de opioides, incluidos CAM-despertar
y CAM-BAR
118,140,141 ,se encontraron resultados comparables: se
producía un efecto techo del opioide a concentraciones plasmáticas
equilibradas definidas.
Signos clínicos de una anestesia y una concentración
plasmática de opioides inadecuadas
Ausems y cols
. 142utilizaron conceptos del modelo farmacodiná-
mico para relacionar los signos clínicos de la anestesia con opioides
inadecuada con las concentraciones plasmáticas del fármaco. En el
paradigma de su estudio, los pacientes se premedicaron con una
benzodiazepina,laanestesiafueinducidaconalfentanilo(150
m
g/kg)
y se intubó la tráquea con ayuda de succinilcolina. La anestesia se
mantuvo con un 70% de óxido nitroso y una infusión variable de
alfentanilo. La infusión se ajustó para controlar las siguientes varia-
bles clínicas: 1) aumento de la presión arterial sistémica a más de
15 mmHg por encima del valor normal del paciente, 2) aumento
de la frecuencia cardíaca por encima de 90 latidos/minuto en
ausencia de hipovolemia, 3) las respuestas somáticas, como los
movimientos del cuerpo (la parálisis muscular mínima permitía el
movimiento físico), deglución, tos, hacer muecas o abrir los ojos y
4) los signos autónomos de una anestesia inadecuada (p. ej., lagri-
meo, enrojecimiento o sudoración). Si se producía cualquier señal
clínica, se incrementaba la infusión de 25 a 50
m
g/kg/h, y se admi-
nistraba una pequeña dosis del bolo (7
m
g/kg). En todos los pacien-
tes se consiguió un buen control hemodinámico. Sin embargo, si
no se producían signos clínicos, la proporción de infusión se
disminuía a intervalos regulares de 15 minutos.
En la
figura 29-17 Ase muestra la relación entre la concen-
tración plasmática de alfentanilo y la respuesta/sin respuesta para
Monitorización de la profundidad de la anestesia
1013
29
Sección III
Control de la anestesia
© ELSEVIER. Fotocopiar sin autorización es un delito
Figura 29-16
Reducción porcentual de la concentración alveolar mínima
(CAM) de enflurano en función de las concentraciones plasmáticas de
fentanilo. Cada punto representa la concentración media (±EEM) de fentanilo
en el plasma y la reducción porcentual media (±EEM) de la CAM de enflurano.
Los números de perros debajo de las barras del error estándar verticales
indican los números por puntos de datos. EE, error estándar.
(De Murphy MR,
Hug CC Jr: The anesthetic potency of fentanyl in terms of its reduction of
enflurane MAC.
Anesthesiology
57:485-488, 1982.)









